
����������Ƥ�����Ƶ���Ҫ��ѧ�Լ���������ˮâ����Na2SO4����̿���ڸ����·�Ӧ���Ƶã���Ӧʽ���£�
�� Na2SO4 + 4C ���� �� Na2S + 4CO
�� Na2SO4 + 4 CO���� �� Na2S + 4CO2
(1)��Ҫ��ȡNa2S 7.8�ˣ���Ҫ��ˮâ����Na2SO4�� g��
(2)���ڷ�Ӧ�����ɵ�Na2S���ʵ���Ϊ1 mol�������ĵ�̼���ʵ����ʵ�����Χn�ķ�Χ�� < n < ��
(3)����������Ӧ�����ĵ�̼����Ϊ1mol������Na2S�����ʵ���Ϊ y mol�����ɵ�CO��CO2�����ʵ���֮��Ϊx����y��x�Ĺ�ϵʽΪy= ��
(4)Na2S�����ڿ����У��Ỻ��������Na2SO3��Na2SO4���ֳ�ȡ�Ѿ�����������������39.2 g����ˮ�У������������ᣬ��ַ�Ӧ���˵ó���9.6g���ų�H2S����1.12L(��״��)����39.2g������������������Na2S�����ʵ���Ϊ mol��Na2SO3�����ʵ���Ϊ mol��Na2SO4�����ʵ���Ϊ mol��
 �ο�������ϵ�д�
�ο�������ϵ�д� ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| ���� |
| x+2 |
| 4+4x |
| x+2 |
| 4+4x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���Ϻ��г����ظ����߿�ģ�⿼�ԣ���ģ����ѧ�Ծ����������� ���ͣ�������
(��16��)��������������Ƥ�����Ƶ���Ҫ��ѧ�Լ���������ˮâ����Na2SO4����̿���ڸ����·�Ӧ���Ƶã���Ӧʽ���£�
������ Na2SO4 4C
4C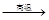 Na2S
Na2S 4CO��
4CO��
������ Na2SO4 4CO
4CO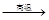 Na2S
Na2S 4CO2
4CO2
��1������Ҫ��ȡNa2S 7.80 g����������������ˮâ����Na2SO4����������Ϊ90%������������Ҫ��ˮâ����Na2SO4������������g����ȷ��0.01����
��2�������ڷ�Ӧ�����ɵ�Na2S���ʵ���Ϊ1 mol�������ĵ�̼���ʵ����ʵ���n�ķ�Χ��
���������� ��n������������ ��
��3��������������Ӧ�����ĵ�̼����Ϊ1 mol������Na2S�����ʵ���Ϊ y mol�����ɵ�CO��CO2�����ʵ���֮��Ϊx����y��x�Ĺ�ϵʽΪy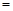 ���� ��������
���� ��������
��4����Na2S�����ڿ����У��Ỻ��������Na2SO3��Na2SO4���ֳ�ȡ�Ѿ�����������������Ʒ39.20 g����ˮ�У������������ᣬ��ַ�Ӧ���˵ó���9.6 g���ų�H2S����1.12 L����״����������㣺39.20 g��Ʒ�и��ɷֵ����ʵ����ֱ�Ϊ���� �� ����
��������д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012����У�Ϻ��У�����������ʦ������У�����������ѧ�Ծ����������� ���ͣ�������
�����10�֣�
����������Ƥ�����Ƶ���Ҫ��ѧ�Լ���������ˮâ����Na2SO4����̿���ڸ����·�Ӧ���Ƶã���Ӧʽ���£�Na2SO4+ 4C Na2S+4CO�� �� Na2SO4+4CO
Na2S+4CO�� �� Na2SO4+4CO Na2S+4CO2
Na2S+4CO2
��1����Ҫ��ȡNa2S 7.80 g����������������ˮâ����Na2SO4����������Ϊ90%������������Ҫ��ˮâ����Na2SO4�� g����ȷ��0.01����
��2�����ڷ�Ӧ�����ɵ�Na2S���ʵ���Ϊ1 mol�������ĵ�̼���ʵ����ʵ���n�ķ�Χ��
�� n �� ��
��3������������Ӧ�����ĵ�̼����Ϊ1 mol������Na2S�����ʵ���Ϊy mol�����ɵ�CO��CO2�����ʵ���֮��Ϊx����y��x�Ĺ�ϵʽΪy= ��
��4��Na2S�����ڿ����У��ᱻ����������Na2SO3��Na2SO4���ֳ�ȡ�Ѿ�����������������Ʒ39.20 g����ˮ�У������������ᣬ��ַ�Ӧ����˵ó���9.6 g���ų�H2S����1.12 L����״����������㣺39.20 g��Ʒ�и�������������ʵ�����������������ˮ�е��ܽ⣩��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com