
【题目】如果我们规定12C的相对原子质量为24,且0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),那么下列几种物理量不能发生变化的是: ①一个12C原子的质量 ②阿伏加德罗常数(NA)③摩尔质量④O2的相对分子质量⑤气体摩尔体积⑥![]() gC2H5OH的物质的量⑦98%(
gC2H5OH的物质的量⑦98%( ![]() )硫酸的物质的量浓度⑧44gCO2所含的分子个数
)硫酸的物质的量浓度⑧44gCO2所含的分子个数
A. ②③④ B. ①⑧ C. ①②⑦⑧ D. ①⑤⑧
【答案】B
【解析】假设12C的相对原子质量为24,且以0.024千克12C所含有的原子数为阿伏加德罗常数,则在规定12C的相对原子质量为24时,实际上是把作为相对原子质量的标准从原来用12C质量的![]() 改为
改为![]() ,但是单个碳原子的质量并没有因此而发生改变;原来是以0.012kg12C所含有的碳原子数作为阿伏加德罗常数(即6.02×1023),现在用0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),很明显0.024kg12C中所含的原子个数是0.012kg12C中所含的原子个数的2倍;故阿伏加德罗常数(NA)变为原来阿伏加德罗常数的2倍(即2×6.02×1023)。①一个12C原子的质量没有发生改变,故符合;②把作为相对原子质量的标准从原来用12C质量的
,但是单个碳原子的质量并没有因此而发生改变;原来是以0.012kg12C所含有的碳原子数作为阿伏加德罗常数(即6.02×1023),现在用0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),很明显0.024kg12C中所含的原子个数是0.012kg12C中所含的原子个数的2倍;故阿伏加德罗常数(NA)变为原来阿伏加德罗常数的2倍(即2×6.02×1023)。①一个12C原子的质量没有发生改变,故符合;②把作为相对原子质量的标准从原来用12C质量的![]() 改为
改为![]() ,但是单个碳原子的质量并没有因此而发生改变,原来是以0.012kg12C所含有的碳原子数作为阿伏加德罗常数(即6.02×1023),现在用0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),很明显0.024kg12C中所含的原子个数是0.012kg12C中所含的原子个数的2倍,故阿伏加德罗常数(NA)变为原来阿伏加德罗常数的2倍(即2×6.02×1023),故不符合;③一个分子或原子的质量不变,阿伏伽德罗常数变为原来的2倍,则摩尔质量变为原来的2倍,故不符合;④氧原子质量不变,但标准却由12C质量的
,但是单个碳原子的质量并没有因此而发生改变,原来是以0.012kg12C所含有的碳原子数作为阿伏加德罗常数(即6.02×1023),现在用0.024kg12C中所含的原子个数为阿伏加德罗常数(NA),很明显0.024kg12C中所含的原子个数是0.012kg12C中所含的原子个数的2倍,故阿伏加德罗常数(NA)变为原来阿伏加德罗常数的2倍(即2×6.02×1023),故不符合;③一个分子或原子的质量不变,阿伏伽德罗常数变为原来的2倍,则摩尔质量变为原来的2倍,故不符合;④氧原子质量不变,但标准却由12C质量的![]() 改为
改为![]() ,所以氧原子的相对原子质量由16变为32,故氧气分子的相对分子质量变为原来的2倍,故不符合;⑤阿伏伽德罗常数变为原来的2倍,则每摩尔气体含有的分子数目为原来的2倍,一定条件下占有的体积为原来的2倍,故不符合;⑥C2H5OH的摩尔质量变为原来的2倍,故ag乙醇的物质的量变为原来的
,所以氧原子的相对原子质量由16变为32,故氧气分子的相对分子质量变为原来的2倍,故不符合;⑤阿伏伽德罗常数变为原来的2倍,则每摩尔气体含有的分子数目为原来的2倍,一定条件下占有的体积为原来的2倍,故不符合;⑥C2H5OH的摩尔质量变为原来的2倍,故ag乙醇的物质的量变为原来的![]() ,故不符合;⑦阿伏加德罗常数(NA)变为原来阿伏加德罗常数的2倍,浓硫酸(98%)的物质的量浓度变为原来2倍,故不符合;⑧一个CO2分子的质量不变,故44g CO2所含的分子个数不变,故符合;故选B。
,故不符合;⑦阿伏加德罗常数(NA)变为原来阿伏加德罗常数的2倍,浓硫酸(98%)的物质的量浓度变为原来2倍,故不符合;⑧一个CO2分子的质量不变,故44g CO2所含的分子个数不变,故符合;故选B。


科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.干冰升华要吸收大量的热,属于化学反应中的吸热反应
B.人们用氧炔焰焊接或切割金属,主要是利用了乙炔燃烧时所放出的热量
C.木炭常温下不燃烧,加热才能燃烧,说明木炭燃烧是吸热反应
D.NaOH固体溶于水后温度升高,说明NaOH的溶解只有放热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施中,不能增大化学反应速率的的是
A.Zn与稀硫酸反应制取H2时,加入蒸馏水
B.Al在O2中燃烧生成Al2O3时,用铝粉替代铝片
C.CaCO3与稀盐酸反应生成CO2时,适当升高温度
D.用KClO3固体分解制取O2时,固体中添加少量MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠具有强碱性和强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法中不正确的是
A. Na2O2与炭、铝粉等还原性物质的燃烧实验可以在硬质玻璃管中进行
B. Na2O2与木炭的反应时Na2O2表现出强氧化性
C. Na2O2与Al反应的方程式为:2Al + 3Na2O2![]() 3 Na2O + Al2O3
3 Na2O + Al2O3
D. Na2O2与SO2反应可生成Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是( ) 
A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液中羟基和羧基均能电离出氢离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C6H14的各种同分异构体中所含甲基数和它的一氯取代物的数目分别是( )
A.2个甲基,能生成4种一氯代物
B.4个甲基,能生成1种一氯代物
C.3个甲基,能生成5种一氯代物
D.4个甲基,能生成4种一氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某纯碱试样中含有 NaCl 杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
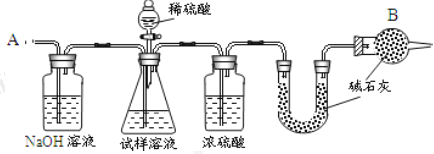
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性;
②将 a g 试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
③称量盛有碱石灰的 U 形管的质量,得到 b g;
④从分液漏斗滴入 6 molL-1的硫酸,直到不再产生气体时为止;
⑤从导管 A 处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的 U 型管的质量,得到 c g;
⑦重复步骤⑤和⑥的操作,直到 U 型管的质量基本不变,为 d g;
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明_________________。
(2)装置中干燥管 B 的作用是______________________。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果_________(填偏高、偏低或不变)。
(4)步骤⑤的目的是__________________________。
(5)步骤⑦的目的是__________________________。
(6)该试样中纯碱的质量分数的计算式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置进行相应实验,能达到实验目的是( )
A.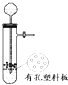 图所示装置用于Cu和浓H2SO4反应制取少量的SO2气体
图所示装置用于Cu和浓H2SO4反应制取少量的SO2气体
B.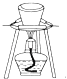 图所示装置用于除去碳酸氢钠固体中的少量碳酸钠
图所示装置用于除去碳酸氢钠固体中的少量碳酸钠
C.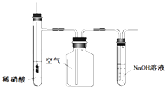 图所示装置用于制备并收集NO气体
图所示装置用于制备并收集NO气体
D.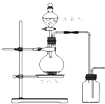 图所示装置制取并收集氨气
图所示装置制取并收集氨气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com