
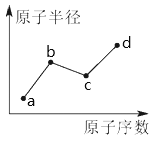
【题目】a、b、c、d是四种常见的短周期主族元素,其原子半径随原子序数的变化如下图所示。已知b、c两种元素的单质是空气的主要成分,d原子的最外层电子数与Ne原子的最外层电子数相差2。下列说法正确的是
A. b、c、d处于同一周期
B. 氢化物的稳定性:d>c
C. a、c、d可形成强弱程度不同的含氧酸
D. b、d的最简单氢化物可相互化合形成共价化合物
【答案】C
【解析】X、Y、Z、W是四种常见的短周期元素,b、c两种元素的单质是空气的主要成分,c的原子序数大于b,可推知c为O、b为N,d原子的最外层电子数与Ne原子的最外层电子数相差2,则W最外层电子数为6,原子半径大于O原子半径,故W为S元素;a的原子序数小于N元素,而原子半径小于N原子,故a为H元素。A.根据上述分析,b、c位于第二正确、d位于第三周期,故A错误;B. 非金属性越强,氢化物越稳定,非金属性O>S,稳定性:c>d,故B错误;C. a、c、d可形成强弱程度不同的含氧酸,如次氯酸和高氯酸等,故C正确;D. b、d的最简单氢化物分别为氨气和氯化氢,相互化合形成氯化铵,属于离子化合物,故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】下列有关元素性质的递变规律不正确的是
A. Na、Mg、Al的金属性依次减弱 B. H2S、H2O、HF的稳定性依次减弱
C. Cl-、Br-、I-还原性依次增强 D. Na、K、Rb的原子半径依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠是一种重要的化工原料,主要采用氨碱法生产。回答下列问题:
(1)碳酸钠俗称________,可作为碱使用的原因是___________(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g)= Na2CO3(s)+H2O(g) ΔH1=127.4 kJ·mol1
②NaOH(s)+CO2(g)= NaHCO3(s) ΔH1=131.5 kJ·mol1
反应2NaHCO3(s)= Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=_______ kJ·mol1,该反应的平衡常数表达式K=________。
(3)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中![]() =_____________。已知Ksp(BaCO3)=2.6×109,Ksp(BaSO4)=1.1×1010。
=_____________。已知Ksp(BaCO3)=2.6×109,Ksp(BaSO4)=1.1×1010。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用等体积的0.1mol/L的BaCl2 溶液,可使相同体积的Fe2 (SO4 )3 、Na2 SO4 、KAl(SO4)2 三种溶液中的SO42-完全沉淀,则三种硫酸盐的物质的量浓度之比为( )
A. 3:2:3 B. 3:1:2 C. 2:6:3 D. 1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是:
A. l6O与 l8O的转化可以通过化学反应实现
B. 灼烧氯化钠时火焰呈黄色,那是发生了化学反应
C. 碱性氧化物一定是金属氧化物
D. 只由一种元素组成的物质一定是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两种化合物的结构或性质描述正确的是

A. 两种物质可用滴有酚酞的NaOH溶液来区分
B. 两种物质的分子式皆为C10H12O2,二者互为同分异构体
C. 两种物质均能发生加成反应、取代反应、酯化反应、氧化反应
D. 两物质都含有不饱和键,因此都能使溴的四氯化碳溶液因发生加成反应而褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 煤的干馏、煤的气化和液化都是化学变化,石油的分馏是物理变化
B. 葡萄糖与果糖、淀粉与纤维素分子式相同结构不同,均互为同分异构体
C. 只有一种元素组成的物质一定是纯净物
D. 单质硅可用于制造硅太阳能电池以及光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A元素的一种同位素,比镤91—239的原子核内少54个质子和100个中子,则A元素在周期表中的位置是( )
A.第3周期第ⅠA族B.第4周期第ⅠA族
C.第5周期第ⅠA族D.第3周期第ⅡA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com