
·ÖĪö £Ø1£©øł¾Ż»ÆѧŹ½øÄŠ“³ÉĻąÓ¦µÄŃõ»ÆĪļµĆŠĪŹ½£¬°“ÕÕ»īĘĆ½šŹōŃõ»ÆĪļ£®½Ļ»īĘĆ½šŹōŃõ»ÆĪļ£®SiO2£®H2OµĆĖ³ŠņĄ“ŹéŠ“£¬²¢ŅŖ×ńŹŲŌ×ÓŹŲŗ楓·ÖĪö½ā“š£»
£Ø2£©ĒāŃõ»ÆĀĮŗĶŃĪĖį·“Ӧɜ³ÉČżĀČ»ÆĀĮŗĶĖ®£»Š”ĖÕ“ņ£ØNaHCO3£©ŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘ”¢Ė®ŗĶ¶žŃõ»ÆĢ¼£»
£Ø3£©²£Į§ÖŠŗ¬ÓŠ¶žŃõ»Æ¹č£¬¶žŃõ»Æ¹čŗĶĒā·śĖį·“Ӧɜ³ÉĖÄ·ś»Æ¹č£»
£Ø4£©ĀČĖįÄĘŗĶÅØŃĪĖį·“Ó¦ÄÜÉś³É¶žŃõ»ÆĀČ”¢ĀČĘų”¢Ė®ŗĶĀČ»ÆÄĘ£®
½ā“š ½ā£ŗ£Ø1£©ĀĮµÄŃõ»ÆĪļĪŖAl2O3£¬¹čµÄŃõ»ÆĪļĪŖSiO2£¬ĒāµÄŃõ»ÆĪļĪŖH2O£¬
Ōņøł¾Ż»īĘĆ½šŹōŃõ»ÆĪļ£®½Ļ»īĘĆ½šŹōŃõ»ÆĪļ£®SiO2£®H2OµĆĖ³ŠņæÉÖŖ£¬
Õ³ĶĮ[Ö÷ŅŖ³É·ÖAl2Si2O5£ØOH£©4]æÉøijÉAl2O3.2SiO2.2H2O£¬
¹Ź“š°øĪŖ£ŗAl2O3.2SiO2.2H2O£»
£Ø2£©ĒāŃõ»ÆĀĮŗĶŃĪĖį·“Ӧɜ³ÉČżĀČ»ÆĀĮŗĶĖ®£ŗAl£ØOH£©3+HCl=AlCl3+H2O£¬Š”ĖÕ“ņ£ØNaHCO3£©ŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘĖ®ŗĶ¶žŃõ»ÆĢ¼£ŗNaHCO3+HCl=NaCl+H2O+CO2”ü£¬Éś³É¶žŃõ»ÆĢ¼»įŅżĘšĪø“©æ×£¬
¹Ź“š°øĪŖ£ŗAl£ØOH£©3£»NaHCO3£»
£Ø3£©²£Į§ÖŠŗ¬ÓŠ¶žŃõ»Æ¹č£¬¶žŃõ»Æ¹čŗĶĒā·śĖį·“Ӧɜ³ÉĖÄ·ś»Æ¹č£¬·“Ó¦·½³ĢŹ½ĪŖSiO2+4HF=SiF4”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗSiO2+4HF=SiF4”ü+2H2O£»
£Ø4£©ÓĆNaClO3Ńõ»ÆÅØŃĪĖįÖĘČ”ClO2£¬Ķ¬Ź±ÓŠCl2Éś³É£¬ĒŅCl2Ģå»żĪŖClO2µÄŅ»°ė£¬ĀČĖįÄĘŗĶÅØŃĪĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2NaClO3+4HCl=2ClO2”ü+Cl2”ü+2H2O+2NaCl£¬
¹Ź“š°øĪŖ£ŗ2NaClO3+4HCl£ØÅØ£©=Cl2”ü+2ClO2+2NaCl+2H2O£®
µćĘĄ ±¾Ģā漲齫ø“ŌÓ»ÆŗĻĪļŠ“³öŃõ»ÆĪļµÄŠĪŹ½”¢·½³ĢŹ½ŹĒŹéŠ“£¬Ć÷Č·ĪļÖŹµÄŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬øł¾Ż·“Ó¦Īļ”¢Éś³ÉĪļ¼°·“Ó¦Ģõ¼žŹéŠ“·½³ĢŹ½£¬ĢāÄæÄŃ¶Č²»“󣬲ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
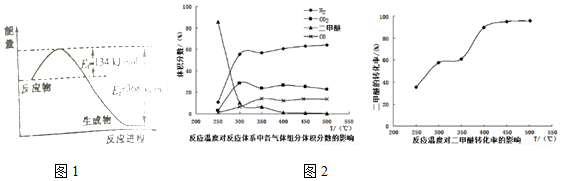
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 11.4g | B£® | 14.8g | C£® | 205g | D£® | ĪŽ·Ø¼ĘĖć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4CO+Fe3O4$\frac{\underline{\;øßĪĀ\;}}{\;}$Fe+4CO2 | B£® | 2KClO3$\frac{\underline{MnO_2}}{”÷}$2KCl+3O2”ü | ||
| C£® | Zn+H2SO4ØTZnSO4+H2”ü | D£® | CH4+2O2$\frac{\underline{\;µćČ¼\;}}{\;}$CO2+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«Al2O3¹ĢĢå·ŪÄ©¼Óµ½·ŠĖ®ÖŠ | |
| B£® | ½«CO2ĘųĢå²»¶ĻĶØČĖµ½NaAlO2ČÜŅŗÖŠ | |
| C£® | ½«¹żĮæµÄ½šŹōÄĘĶ¶Čėµ½NaAlO2ČÜŅŗÖŠ | |
| D£® | Ļņ340ml 1mol/L NaOHČÜŅŗÖŠ¼ÓČė80ml 1mol/LµÄAlCl3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
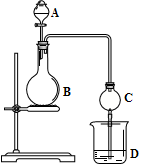 »ÆѧŹµŃéÖŠ£¬Ķ¬Ņ»øö×°ÖĆæÉŅŌÓĆÓŚ²»Ķ¬µÄŹµŃ飬ĄżČēĶ¼µÄŹµŃé×°ÖĆ£ØBÖŠæÉĪŖ¹ĢĢå»ņŅŗĢ壬æɼÓČČ£©£®
»ÆѧŹµŃéÖŠ£¬Ķ¬Ņ»øö×°ÖĆæÉŅŌÓĆÓŚ²»Ķ¬µÄŹµŃ飬ĄżČēĶ¼µÄŹµŃé×°ÖĆ£ØBÖŠæÉĪŖ¹ĢĢå»ņŅŗĢ壬æɼÓČČ£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ÅäÖĘČÜŅŗ | B£® |  ÖŠŗĶµĪ¶Ø | ||
| C£® |  ³żČ„äå±½ÖŠÉŁĮæµÄäåµ„ÖŹ | D£® |  ÖĘČ”²¢ŹÕ¼Æ°±Ęų |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com