
(6分)将12.4g钠和过氧化钠混合物完全溶于水中得100mL溶液,所收集的气体在一定条件下恰好完全反应,则所得溶液的物质的量浓度是多大?(写出计算过程)
科目:高中化学 来源:2015-2015湖南省高二12月学科联赛化学试卷(解析版) 题型:填空题
18.(12分)甲醇可通过将煤的气化过程中生成的CO 和H2在一定条件下发生如下反应制得:CO(g) + 2H2(g)=CH3OH(g)
请根据下图回答下列问题:

(1)从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=____mol / (L·min)。
(2)写出该反应的热化学方程式_____________________________________________________
(3)恒容条件下,下列措施中能使 n(CO) /n(CH3OH)增大的有 。
A.升高温度 B.充入He气
C.再充入1 mol CO和2 mol H2 D.使用催化剂
(4)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化(Q1、Q2、Q3均大于0) |
甲 | 1 mol CO和2 mol H2 | a1 | c1 | 放出Q1kJ热量 |
乙 | 1 mol CH3OH | a2 | c2 | 吸收Q2kJ热量 |
丙 | 2mol CO和4 mol H2 | a3 | c3 | 放出Q3kJ热量 |
则下列关系正确的是:
A. c1=c2
B.2Q1=Q3
C.2a1=a3
D.a1+ a3=1
E.该反应若生成1 mol CH3OH,则放出(Q1+ Q2)kJ热量
(5)若在一体积可变的密闭容器中充入1 mol CO、2 mol H2和1 mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向 (填“正”、“逆”)反应方向移动,理由是由质量守恒,密度为原来的1.6倍,所以体积缩小,平衡正移。
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高二上学期第二次统练化学试卷(解析版) 题型:选择题
4.常温下在水中加入下列物质,不会破坏水的电离平衡的是
A.通入HCl气体 B.加入氨水 C.加入乙醇 D.加入金属钠
查看答案和解析>>
科目:高中化学 来源:2014-2015云南省景洪市高一上学期期中化学试卷(解析版) 题型:选择题
12.用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4LH20含有的分子数为NA
B.常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA
C.通常状况下,NA个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源:2014-2015云南省景洪市高一上学期期中化学试卷(解析版) 题型:选择题
5、下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
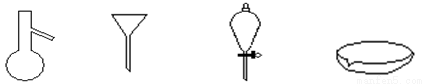
A、蒸馏、过滤、萃取、蒸发 B、蒸馏、蒸发、萃取、过滤
C、萃取、过滤、蒸馏、蒸发 D、过滤、蒸发、萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省文登市高一上学期期末考试化学试卷(解析版) 题型:填空题
(6分)下表为各物质中所含有的少量杂质,在空格处填写除杂所用试剂和操作方法。
序号 | 物质 | 杂质 | 除杂质试剂 | 操作方法 |
① | Fe(OH)3胶体[ | Na+、Cl- | 水 | |
② | FeSO4溶液 | CuSO4 | ||
③ | CO2 | HCl | 洗气 | |
④ | NaCl溶液 | I2 |
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省文登市高一上学期期末考试化学试卷(解析版) 题型:选择题
已知磷单质在KOH溶液中的变化是:4P+3KOH+3H2O=3KH2PO2+PH3↑,下列说法正确的是
A.该反应中P做还原剂,H2O作氧化剂
B.该反应中氧化产物和还原产物的物质的量比为1:3
C.每有1mol P参加反应,转移0.75mol电子
D.该反应每转移0.3mol电子,就有2.24L PH3气体生成
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省文登市高二上学期期末考试化学试卷(解析版) 题型:填空题
(6分)(1)相同物质的量的①C2H4 ②C2H6O完全燃烧,消耗氧气物质的量关系为______(填编号,用“>”或“=”表示)。
(2) 的分子式为______________。
的分子式为______________。
(3)在1个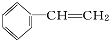 分子中,处于同一平面上的原子数最多可能有____个。
分子中,处于同一平面上的原子数最多可能有____个。
(4)1mol醛基与足量银氨溶液完全反应生成Ag的物质的量为________。
(5)高聚物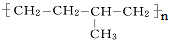 的单体为__________、___________。
的单体为__________、___________。
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省临沂市高二上学期期末化学试卷(解析版) 题型:填空题
(12分)铜及其化合物在工农业生产及日常生活中应用非常广泛。某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2.2H2O)的流程如下。

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
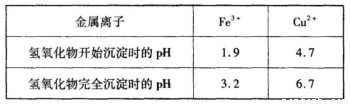
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质。
①试剂X可选用下列物质中的__________(填代号)。
a.CuO b.NaOH c.Cu d.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是__________。
(2)由溶液Ⅱ制备CuCl2.2H2O的操作依次为:边滴加浓盐酸边加热浓缩、__________(填操作名称)、过滤、洗涤干燥。
(3)向溶液Ⅱ中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因:__________.
(4)某学习小组用碘量法测定CuCl2.2H2O样品的纯度(杂质不与发生反应)。实验如下:
a.准确称取CuCl2.2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250 mL待测溶液。(已知: )
)
b.移取25. 00 mL待测溶液于锥形瓶中,加几滴指示剂,用c mol Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。 (已知:
Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。 (已知: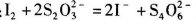 )
)
①实验中使用的指示剂名称为____________。
②达到滴定终点时,仰视滴定管读数将使测定结果_________(填“偏高”、“偏低”或“无影响”)。
③该样品中CuCl2.2H2O 的质量分数为_________(用含m、c、V的代数式表示,不用化简)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com