
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |

分析 (1)平衡常数=$\frac{生成物平衡浓度的幂次方乘积}{反应物的平衡浓度幂次方乘积}$,注意固体和纯液体不能写入表达式;
(2)由表中数据可知,升高温度,平衡常数增大,反应向正反应方向移动,据此判断;
(3)根据平衡移动原理方向解答;
(4)A、由图可知,升高温度,平衡向正反应移动,故图象表示正反应吸热反应,结合反应①的热效应判断;
B、由图可知,最高点到达平衡,温度升高,混合物中CO的含量降低,平衡向逆反应进行,故图象表示正反应为放热反应,结合反应①的热效应判断;
C、由图可知,温度T1先到达平衡,故温度T1>T2,温度T1到达平衡时,混合物中CO的含量降低,平衡向逆反应进行,故图象表示正反应为放热反应,结合反应①的热效应判断;
解答 解:(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=akJ•mol-1,固体不写入平衡常数表达式,则平衡常数K=$\frac{[CO]}{[C{O}_{2}]}$,
故答案为:$\frac{[CO]}{[C{O}_{2}]}$;
(2)由表中数据可知,升高温度,平衡常数增大,反应向正反应方向移动,则正反应为吸热反应,即a>0,
故答案为:吸热;
(3)A.反应是前后气体体积不变的反应,缩小反应器体积,体系的压强增大,但平衡不移动,故A错误;
B.通入CO2,增大反应物浓度平衡向正反应方向移动,故B正确;
C.图表数据可知,升高温度到900℃,平衡常数增大,平衡向正反应方向移动,故C正确;
D.使用合适的催化剂,只能加快反应速率,同等程度增大正逆反应速率,平衡不移动,故D错误;
E、固体对平衡无影响,增加Fe的量对平衡无影响,故E错误;
故答案为:BC;
(4)A、由图可知,升高温度,平衡向正反应移动,故图象表示正反应吸热反应,反应①正反应是吸热反应,图象与实际相符合,故A正确;
B、由图可知,最高点到达平衡,温度升高,混合物中CO的含量降低,平衡向逆反应进行,故图象表示正反应为放热反应,反应①正反应是吸热反应,图象与实际不相符,故B错误;
C、由图可知,温度T1先到达平衡,故温度T1>T2,温度T1到达平衡时,混合物中CO的含量降低,平衡向逆反应进行,故图象表示正反应为放热反应,反应①正反应是吸热反应,图象与实际不相符,故C错误;
故答案为:A.
点评 本题目综合性较大,涉及反应速率、平衡常数、化学平衡计算,影响反应速率与化学平衡移动的因素分析等,平衡移动原理的理解应用是解题关键,难度中等.


科目:高中化学 来源: 题型:解答题
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 1.8 | 6.3 | 5.2 |
| 完全沉淀的pH | 3.0 | 8.3 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀KOH溶液 | B. | HCl溶液 | C. | CuSO4溶液 | D. | NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①④ | D. | 只有④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,有机物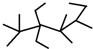 的命名为2,2,4,4,5-五甲基-3,3-二乙基庚烷 的命名为2,2,4,4,5-五甲基-3,3-二乙基庚烷 | |
| B. | 乙醇发生消去反应、乙醇氧化为乙醛、乙酸的酯化反应中均是C-O键发生断裂 | |
| C. | C3H6和C4H8在分子组成上相差CH2,所以二者互为同系物 | |
| D. | 荧光黄结构为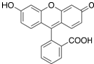 ,其分子式为C20H12O5,其中最多有9个碳原子共平面 ,其分子式为C20H12O5,其中最多有9个碳原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
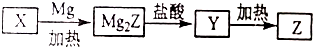
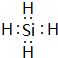 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com