
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
已知热化学方程式2C2H2 (g) + 5O2 (g)= 4CO2 (g) +2H2O (g) ΔH= -1256 kJ/mol,下列说法正确的是
A.乙炔的燃烧热为1256 kJ /mol
B.若转移10 mol电子,则消耗2.5 mol O2
C.若生成2 mol 液态水,则ΔH = -1256 kJ/mol
D.若形成4 mol碳氧共用电子对,则放出的热量为1256 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
有原子序数均小于20的A、B、C、D四种元素,已知:① A和B在同一主族,C和D在同一周期;② 四元素相互间可形成A2C、A2C2、B2C2、DC2等化合物;③ B的阳离子与C的阴离子核外电子层结构相同;④B2C2与A2C或DC2反应都生成C2气体;⑤ B的单质与A2C反应生成A2气体,A2与C2混合遇火可发生爆炸,生成常温下无色、无味的液体A2C.试回答:
(1)写出A和D两元素的名称:A________、D________
(2)画出B离子和C离子的结构示意图_____________ , _____________ 。
两种离子中,半径较小的是________(填离子符号)。
(3)写出A2C2、B2C2的电子式:A2C2__________ B2C2__________
(4)写出B2C2与DC2反应的化学方程式________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的性质呈周期性变化的根本原因是
A.元素的相对原子质量呈周期性变化 B.元素的原子半径呈周期性变化
C.元素的金属性和非金属性呈周期性变化 D.元素原子的核外电子排布呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
对反应4A+5B == 4C+6D,以下化学反应速率的表示中,所表示反应速率最快的是
A. v (A)=0.40mol•L-1•s-1 B. v (B)=0.48mol•L-1•s-1
C. v (C)=0.36mol•L-1•s-1 D. v (D)=0.55mol•L-1•s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于铷的叙述中正确的是( )
A.硝酸铷是离子化合物
B.在钠、钾、铷三种单质中,铷的熔点最高
C.氢氧化铷是弱碱
D.它位于周期表的第四周期、第ⅠA族
查看答案和解析>>
科目:高中化学 来源: 题型:
亚硝酸钠(NaNO2)是一种工业盐,实验室可用如下装置(略去部分夹持仪器)制备。
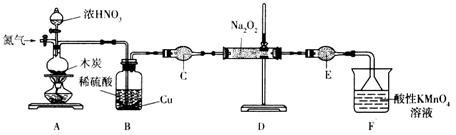
已知:①2NO+Na2O2=2NaNO2;
②3 NaNO2+3HCl=3NaCl+HNO3+2NO↑+H2O;
③酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色。
(1)加热装置A前,先通一段时间N2,目的是_______________。
(2)装置A中发生反应的化学方程式为__________________________________。实验结束后,将B瓶中的溶液经蒸发浓缩、__________(填操作名称)、过滤可获得CuSO4·5H2O。
(3)仪器C的名称为______________,其中盛放的药品为 ____________(填名称)。
(4)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,___________________________,则产物是NaNO2(注明试剂、现象)。
(5)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
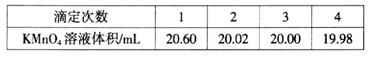
①第一组实验数据出现异常,造成这种异常的原因可能是_________(填代号)。
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时仰视读数
②根据表中数据,计算所得固体中亚硝酸钠的质量分数__________。
(6)设计合理实验比较0.1 mol·L-1NaNO2溶液中NO2-的水解程度和0.1 mol·L-1HNO2溶液中HNO2的电离程度相对大小。(简要说明实验步骤、现象和结论,仪器和药品自选)
___________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com