
【题目】NaCl是基础化工原料,通过电解饱和食盐水可制得NaOH、H2、Cl2。完成下列填空:
(1)写出电解饱和食盐水的化学方程式________________________,阳极产物是 __________,检验该产物的一种简便化学方法是__________________________________。
(2)氯原子结构示意图为_______, 氯离子电子式是_______,氯气所含化学键是_________。
(3)氯气经过压缩后变成液氯,属于__________变化(选填“物理”或“化学”)。常用浓氨水来检查输氯管道是否破损,破损处会形成大量白烟NH4Cl和一种无色无味的单质气体,写出化学方程式并标出电子转移的方向和数目:____________________________________________。
(4)Cl与Br属于同主族元素,这两种元素非金属性较强的是______________,请用一个事实说明你的结论:____________________________________________________ 。
【答案】 2NaCl +2 H2O![]() 2NaOH + Cl2↑ + H2↑ Cl2 湿润的KI淀粉试纸
2NaOH + Cl2↑ + H2↑ Cl2 湿润的KI淀粉试纸 
![]() 共价键 物理
共价键 物理  Cl Cl2 + NaBr → Br2 + 2NaCl或HCl的稳定性强于HBr或高氯酸的酸性强于高溴酸(注:其它合理答案)
Cl Cl2 + NaBr → Br2 + 2NaCl或HCl的稳定性强于HBr或高氯酸的酸性强于高溴酸(注:其它合理答案)
【解析】本题主要考查氯气的性质。
(1)电解饱和食盐水的化学方程式:2NaCl +2 H2O![]() 2NaOH + Cl2↑ + H2↑,阳极产物是 Cl2,检验该产物的一种简便化学方法是湿润的KI淀粉试纸,利用Cl2+2KI
2NaOH + Cl2↑ + H2↑,阳极产物是 Cl2,检验该产物的一种简便化学方法是湿润的KI淀粉试纸,利用Cl2+2KI![]() 2KCl+I2,碘遇淀粉变蓝。
2KCl+I2,碘遇淀粉变蓝。
(2)氯原子结构示意图为![]() , 氯离子电子式是
, 氯离子电子式是![]() ,氯气所含化学键是共价键。
,氯气所含化学键是共价键。
(3)氯气经过压缩后变成液氯,没有生成新物质,属于物理变化。常用浓氨水来检查输氯管道是否破损,破损处会形成大量白烟NH4Cl和一种无色无味的单质气体,该气体是氮气,写出化学方程式并标出电子转移的方向和数目: 。
。
(4)Cl与Br属于同主族元素,同主族元素从上到下非金属性逐渐减弱,所以这两种元素非金属性较强的是Cl,说明此结论的事实可以是:Cl2 + NaBr → Br2 + 2NaCl或HCl的稳定性强于HBr或高氯酸的酸性强于高溴酸。


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】按照无机物的分类方法,下列各组物质中,属于不同类型的物质是( )
A.火碱、烧碱、生石灰
B.生石灰、冰、干冰
C.熟石灰、苛性钠、氢氧化钾
D.纯碱、硫酸钠、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1,若阿伏加德罗常数用NA表示。
①该气体的物质的量为________mol。
②该气体所含原子总数为________个。
③该气体在标准状况下的体积为________
(2)已知有C2H4O、C3H6 O、C4H8 O三种物质的混合物,测得氧元素的质量分数为32%,则混合物中C元素的质量分数为___________________________________________,则混合物中H元素的质量分数为_________________________(保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
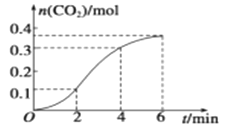
A. 反应在2~4 min内平均反应速率最大
B. 反应开始4 min内温度比浓度对反应速率的影响大
C. 4 min后,反应速率减小的主要原因是c(H+)减小
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在科学史上每一次重大的发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于( )
A.提出了元素周期律
B.开发了合成氨的生产工艺
C.揭示了燃烧的本质
D.提取了治疟药物青蒿素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)常用作催化剂和合成洗涤剂,其沸点为-5.5℃,易水解。某学习小组在实验室中用下图所示装置制备ClNO。已知:HNO2既有氧化性又有还原性;AgNO2微于水,能溶于硝酸,AgNO2+HNO3=AgNO3+HNO2。
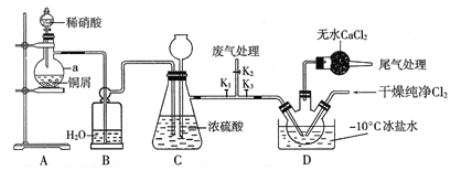
回答下列问题:
(1)仪器a的名称为_____________,装置B的作用是____________。
(2)装置C中长颈漏斗的作用是____________。
(3)实验开始时,先打开K1、K2,关闭K3,再打开分液漏斗活塞滴人适量稀硝酸,当观察到C中______时关闭K1、K2。向装置D三颈瓶中通人千燥纯净Cl2,当瓶中充满黄绿色气体时,再打开K1、K3,制备ClNO。
(4)装置D中干燥管的作用是__________________。
(5)实验过程中,若学习小组同学用酒精灯大火加热制取NO,对本实验造成的不利影响是____、________。
(6)ClNO与H2O反应生成HNO2和HCl。
①设计实验证明HNO2是弱酸________________。(仅提供的试剂:1mol/L盐酸、1mol/L HNO2、Na、NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)
②要验证ClNO与H2O反应后的溶液中存在Cl-和HNO2,合理的操作步骤及正确的顺序是_____(填序号)。
a.向烧杯中滴加过量KI淀粉溶液,溶液变蓝色
b.取1.0mL三颈瓶中产品于烧杯中,加入10.0mLH2O充分反应
c.向烧杯中滴加酸性KMnO4溶液,溶液紫色褪去
d.向烧杯中滴加足量AgNO3溶液,有白色沉淀生成,加入稀硝酸,搅拌,仍有白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,22.4L.NO和11.2L O2反应,生成气体的分子数目为NA
B. 将CuO和Cu2S等质量混合,混合物中Cu2+数目为NA
C. 1L.pH=12的NaOH溶液中的OH-数目为0.01NA
D. 0.1molT218O所含电子数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com