
| A. | 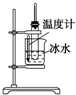 实验室制取少量的硝基苯 | |
| B. | 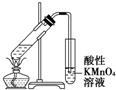 证明溴乙烷、NaOH、乙醇溶液共热生成乙烯 | |
| C. | 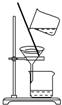 分离乙酸乙酯、碳酸钠和水的混合物 | |
| D. | 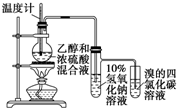 证明乙醇、浓硫酸共热生成乙烯 |
分析 A.制备硝基苯应水浴加热;
B.溴乙烷、NaOH、乙醇溶液发生消去反应生成乙烯,但乙醇挥发,乙醇也能被高锰酸钾氧化;
C.乙酸乙酯、碳酸钠和水的混合物,分层,乙酸乙酯在上层;
D.乙醇和浓硫酸混合加热到170°C发生消去反应生成乙烯,过程中副反应为浓硫酸脱水性得到碳和浓硫酸加热反应生成二氧化碳和二氧化硫,二氧化硫具有还原性和溴单质发生反应,检验乙烯前需要除去二氧化硫.
解答 解:A.制备硝基苯应水浴加热,温度计测定水温度,加热至50℃~60℃,故A错误;
B.溴乙烷、NaOH、乙醇溶液发生消去反应生成乙烯,但乙醇挥发,乙醇也能被高锰酸钾氧化,不能说明乙烯的生成,故B错误;
C.乙酸乙酯、碳酸钠和水的混合物,分层,乙酸乙酯在上层,则利用分液法分离,不能利用过滤分离,故C错误;
D.乙醇和浓硫酸混合加热到170°C发生消去反应生成乙烯,过程中副反应为浓硫酸脱水性得到碳和浓硫酸加热反应生成二氧化碳和二氧化硫,二氧化硫具有还原性和溴单质发生反应,检验乙烯前需要除去二氧化硫,装置中乙烯发生装置正确,通过氢氧化钠溶液吸收生成的二氧化硫和二氧化碳,剩余气体通过溴的四氯化碳溶液褪色证明生成乙烯,实验装置能够达到实验目的,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的制备、混合物分离提纯、物质检验实验等,把握反应原理及实验技能为解答的关键,侧重实验基本技能的考查,注意实验的评价性分析,题目难度中等.


科目:高中化学 来源: 题型:解答题
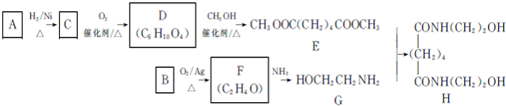
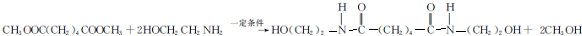 .
.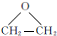 ,能发生银镜反应的F的同分异构体是CH3CHO.
,能发生银镜反应的F的同分异构体是CH3CHO.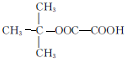 (写结构简式).
(写结构简式).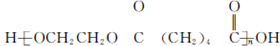 的合成路线:
的合成路线: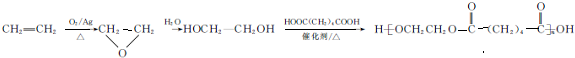 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最易失去的电子能量最高 | |
| B. | 电离能最小的电子能量最高 | |
| C. | 2p轨道电子能量高于2s轨道电子能量 | |
| D. | 在离核最近区域内运动的电子能量最高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
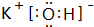 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数A>B | B. | 电子总数A->B2+ | C. | 离子半径A->B2+ | D. | 原子半径A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
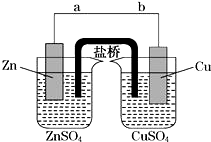 某学生利用如图实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64).按照实验步骤依次回答下列问题:
某学生利用如图实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64).按照实验步骤依次回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
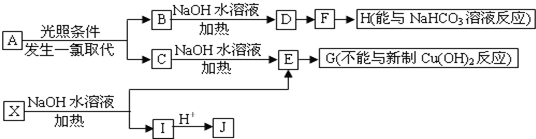
 、
、 、
、 .(不包括A,写结构简式)
.(不包括A,写结构简式) ;反应类型是酯化反应.
;反应类型是酯化反应. +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$ +
+ +H2O
+H2O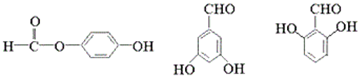 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;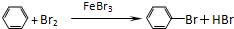 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com