
【题目】四种短周期主族元素X、Y、Z、W的原子序数依次增大。化合物甲由X、Y、Z三种元素组成,25℃时,0.01mol·L-1甲溶液中的![]() ;Z与W同周期,且W的最高正价与最低负价的代数和为4。下列说法中正确的是
;Z与W同周期,且W的最高正价与最低负价的代数和为4。下列说法中正确的是
A. 原子半径:X<Y<Z<W
B. 最简单氢化物的稳定性:Y>W
C. Z分别与Y、W组成的化合物中化学键类型均相同
D. 粘有W的单质的试管可用酒精洗涤
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】H2S是一种剧毒气体,对H2S废气资源化利用途径之一是回收能量并得到单质硫,反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) H=-632kJ·mol-1。下图为质子膜H2S燃料电池的示意图。下列说法错误的是( )

A. 电池工作时,电子从电极a经负载流向电极b
B. 实际工作中当反应生成64gS2时,电池内部释放632kJ电能
C. 电极a上发生的电极反应为:2H2S - 4e-=S2 + 4H+
D. 当电路中通过4mol电子时,有4molH+经质子膜进入正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积一定的密闭容器中加入1 mol N2和3 mol H2发生反应:N2 + 3H2 ![]() 2NH3(正反应是放热反应)。下列有关说法正确的是
2NH3(正反应是放热反应)。下列有关说法正确的是
A.降低温度可以加快反应速率
B.达到化学反应限度时,生成2mol NH3
C.向容器中再加入N2可以加快反应速率
D.1mol N2 和3mol H2的总能量低于2mol NH3的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需用2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是
A.950mL 111.2g B.500mL 117.0g
C.1000mL 117.0g D.1000mL 111.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是无机物A~F在一定条件下的转化关系(部分产物及反应条件未标出)。其中A为气体;A~F都含有相同的元素。

试回答下列问题:
(1)写出下列物质的化学式:C_________、F_________
(2)写出下列反应的化学方程式:
①____________________________________。
③___________________________,该反应氧化剂与还原剂的物质的量之比为_________。
(3)铜与E的浓溶液反应的离子方程式为_________。
(4)25.6g铜与含有1.4 mol E的浓溶液恰好完全反应,最终得到气体的体积为(标准状况下)_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.人们应用原电池原理制作了多种电池,以满足不同的需要,广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应式为_________。电池工作一段时间后需要充电,充电过程中电池液中H2SO4的浓度_____(填“增大”、“减小”或“不变”)。
⑵某学习小组依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计成原电池,则负极发生的电极反应为___________;当反应进行到一段时间后取出电极材料,测得某一电极增重了 5.4g,则该原电池反应共转移了的电子数目是________________________。
⑶燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
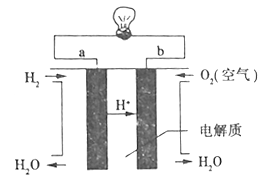
①该电池的正极反应式_________________。
②若该电池的效率80%,当外电路通过0.2mo1电子时,消耗O2的体积____L(标准状况)
II.用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应4HC1+O2 ![]() 2Cl2+2H2O,可实现氯的循环利用。己知上述反应中,4mol HC1被氧化,放出约116kJ的热量。
2Cl2+2H2O,可实现氯的循环利用。己知上述反应中,4mol HC1被氧化,放出约116kJ的热量。
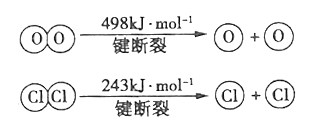
计算断开1 mol H-O键与断开1 mol H-C1键断所吸收能量相差约为______kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.判断下列同分异构属于何种异构?(A、碳链异构B、位置异构C、官能团异构)
①CH3CH=CH(CH2)2CH3和C2H5CH=CHC2H5:
②CH3COOH和HCOOCH3:
Ⅱ.①苯的同系物的通式为CnH2n-6,当出现同分异构体时(同分异构体是苯的同系物),碳原子数的最小值n=
②某气态烷烃的二氯代物有3种,则该烷烃的系统命名为
Ⅲ.某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
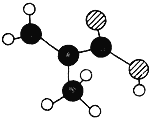
(1)该物质中所含氧官能团的结构简式为_______。
(2)下列物质中,与该物质互为同分异构体的是______
A.CH3CH2CH2COOH B.OHCCH(CH3)CHO C.CH3CH2CH=CHCOOH D.CH2=CHCOOCH3
(3)该分子中最多共平面的原子数为______个。(已知羧基的四个原子可以共平面)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com