
【题目】明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3 杂质。利用明矾石制备氢氧化铝的流程如下:
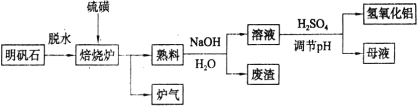
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S=2Al2O3+9SO2,若生成1molAl2O3,则转移的电子数为______。
(2)将标况下1.12L炉气通入100mL0.5mol/LNaOH 溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为______。
(3)熟料溶解时反应的离子方程式为_________。
(4)检验废渣中含有Fe2O3所需的试剂是______________。
(5)母液中溶质主要成分的化学式为_______,溶液调节pH后经过滤、洗涤可得Al(OH)3沉淀,证明沉淀已洗涤干净的实验操作和现象是___________。
【答案】3.612×1024 c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) Al2O3+2OH-=2AlO2-+H2O 稀盐酸、硫氰化钾 K2SO4、Na2SO4 取最后一次洗涤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净
【解析】
(1)所含元素化合价降低的反应物是氧化剂;反应中硫单质中硫元素化合价由0价升高为SO2中+4价,硫单质为还原剂,计算生成1molAl2O3需要硫的物质的量,转移电子是硫单质的4倍,再根据N=nNA转移电子数目;
(2)根据n(SO2):n(NaOH)确定反应产物,再结合溶液呈酸性对离子浓度进行排序;
(3)由工艺流程可知,熟料溶解为氧化铝与氢氧化钠溶液反应生成偏铝酸钠;
(4)由工艺流程可知,废渣的主要成分为Fe2O3,废渣中加入盐酸溶解,再滴加KSCN溶液,若溶液变红色,说明废渣中含有Fe2O3;
(5)由工艺流程可知,熟料溶解所得的溶液中含有K+、Na+、SO42-、AlO2-、OH-等,加硫酸调pH值,AlO2-转化为Al(OH)3,母液中离子主要有K+、Na+、SO42-,据此分析判断。
(1)反应中硫元素化合价由Al2(SO4)3中+6价降低为SO2中+4价,故Al2(SO4)3是氧化剂,反应中硫单质中硫元素化合价由0价升高为SO2中+4价,硫单质为还原剂,生成1molAl2O3需要硫的物质的量为1mol×![]() =1.5mol,转移电子的物质的量为1.5mol×4=6mol,转移电子数目为6mol×6.02×1023mol-1=3.612×1024;
=1.5mol,转移电子的物质的量为1.5mol×4=6mol,转移电子数目为6mol×6.02×1023mol-1=3.612×1024;
(2)标准状况下1.12L二氧化硫的物质的量为 ![]() =0.05mol,n(NaOH)=0.1L×0.5mol/L=0.05mol,n(SO2):n(NaOH)=0.05mol:0.05mol=1:1,故反应后溶液中溶质为NaHSO3,溶液呈酸性,说明HSO3-的电离程度大于水解程度,同时水电离生成氢离子,故c(H+)>c(SO32-),HSO3-电离程度不大,故c(HSO3-)>c(H+),溶液c(OH-)等于水电离生成,浓度很小,故溶液中离子浓度由大到小的排列顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);
=0.05mol,n(NaOH)=0.1L×0.5mol/L=0.05mol,n(SO2):n(NaOH)=0.05mol:0.05mol=1:1,故反应后溶液中溶质为NaHSO3,溶液呈酸性,说明HSO3-的电离程度大于水解程度,同时水电离生成氢离子,故c(H+)>c(SO32-),HSO3-电离程度不大,故c(HSO3-)>c(H+),溶液c(OH-)等于水电离生成,浓度很小,故溶液中离子浓度由大到小的排列顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);
(3)由工艺流程可知,熟料溶解为氧化铝与氢氧化钠溶液反应生成偏铝酸钠,离子方程式为Al2O3+2OH-=2AlO2-+H2O;
(4)由工艺流程可知,废渣的主要成分为Fe2O3,取少量废渣,加入适量盐酸溶解,再滴加KSCN溶液,若溶液变红色,说明废渣中含有Fe2O3,故答案为:稀盐酸、硫氰化钾;
(5)由工艺流程可知,熟料溶解所得的溶液中含有K+、Na+、SO42-、AlO2-、OH-等,加硫酸调pH值,AlO2-转化为Al(OH)3,母液中离子主要有K+、Na+、SO42-,含有溶质为K2SO4、Na2SO4;要证明沉淀已洗涤干净即证明最后的洗涤液中不含SO42-,证明沉淀已洗涤干净的实验操作和现象是:取最后一次洗涤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净;故答案为:K2SO4、Na2SO4;取最后一次洗涤液于试管中,滴加BaCl2溶液,若无白色沉淀生成则已洗涤干净。


科目:高中化学 来源: 题型:
【题目】在273K和101kPa的条件下,将2.00g氦气,1.40g氮气和1.60g氧气混合,求:
(1)该混合气体的总物质的量为______________
(2)该混合气体的体积是_______________
(3)该混合气体的平均摩尔质量为_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向VmL0.1mol/L氨水中滴加等物质的量浓度的稀H2SO4,测得混合溶液的温度和pOH[pOH=-lgc(OH-)]随着加入稀硫酸的体积的变化如图所示(实线为温度变化,虚线为pOH变化),下列说法不正确的是( )
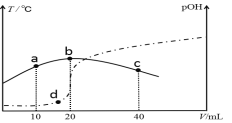
A. a、b、c三点由水电离的c(H+)依次减小
B. V=40
C. b点时溶液的pOH>pH
D. a、b、d三点对应NH3·H2O的电离常数:K(b)>K(d)>K(a)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略混合后溶液的体积变化),实验数据如下表:
实验序号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
请回答:
(1)HA溶液和KOH溶液反应的离子方程式为_____。
(2)下列关于反应后的溶液说法不正确的是____(填字母)。
a.实验②反应后溶液中只存在着两个平衡
b.实验②反应后溶液中:c(A-)+c(HA)>0.1mol·L-1
c.实验②反应后溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
d. 实验①反应后的溶液中由水电离出的c(OH-)=10-9mol·L-1;x>0.2mol·L-1
Ⅱ.已知2H2(g)+O2(g)=2H2O(1) ΔH=-572kJ·mol-1。某氢氧燃料电池以疏松多孔石墨棒为电极,KOH溶液为电解质溶液。
(3)写出该电池工作时负极的电极反应式____。
(4)若该氢氧燃料电池每释放228.8kJ电能时,会生成1mol液态水,则该电池的能量转化率为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向1 L密闭容器中充入3 mol X 气体和1 mol Y气体,发生反应2X(g)+2Y(g)![]() 3Z(g)+2W(g),达到化学平衡时,测出的下列各生成物浓度的数据中肯定错误的是( )
3Z(g)+2W(g),达到化学平衡时,测出的下列各生成物浓度的数据中肯定错误的是( )
A.c(Z)=0.75 mol/LB.c(Z)=1.2 mol/L
C.c(W)=0.8 mol/LD.c(W)=1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一混合物的水溶液,只可能含有以下离子中的若干种:K+、![]() 、Cl-、Mg2+、Ba2+、
、Cl-、Mg2+、Ba2+、![]() 、
、![]() ,现取三份100mL溶液进行如下实验:
,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生;
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测不正确的是
A.K+不一定存在B.100mL溶液中含0.02mol![]()
C.Cl-不一定存在D.Ba2+、Mg2+不存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 1molCO和 2molH2充入一容积为 1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g) ![]() CH3OH(g)。根据图,下列分析中正确的是( )
CH3OH(g)。根据图,下列分析中正确的是( )
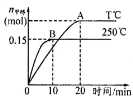
A. 250°C时,反应在前10s的平均速率υ(H2)=0.015mol/(L·min)
B. 平衡时CO的转化率:250°C>T°C
C. 反应达平衡后,其他条件不变,若减小容积体积,CO 体积分数增大
D. 该反应的正反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与加入NaOH溶液的体积关系图如图所示,则混合溶液中Al2(SO4)3和MgSO4的物质的量之比为( )
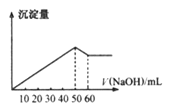
A.6:1B.3:1C.2:1D.1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是短周期的一部分,已知B原子与C 原子核外电子总数之和为A的4倍,则下列推断正确的是

A.A、B、C三者中,A为金属性元素,B、C为非金属性元素
B.A、B、C三者核电荷数之和为40
C.A与B、A与C均可形成离子化合物
D.B与C只能形成一种共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com