

| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
分析 (1)由已知热化学方程式根据盖斯定律构造目标热化学方程式,然后再求热量Q;
(2)①根据温度升高化学平衡向着吸热方向进行;
②根据增加氢气的物质的量化学平衡向着正反应方向移动;
③根据反应物的物质的量之比为等于化学计量数之比时,达平衡状态时生成物的百分含量最大;根据化学平衡状态是反应物的转化率最大、生成物的产率最大来回答;先求出各自的平衡浓度,然后根据平衡常数的概念来回答;
(3)①500s,c(N2O5)变化量为5.00-3.52=1.48mol/L,结合v=$\frac{△c}{△t}$计算,由速率之比等于化学计量数之比求算即可;
②燃料原电池中,负极上燃料失电子发生氧化反应,负极上燃料失电子和碳酸根离子反应生成二氧化碳和水;先根据化合价判断生成N2O5的电极,N2O5中氮元素的化合价是+5价,而硝酸中氮元素也是+5价.因此应该在左侧生成N2O5,即在阳极区域生成,再根据离子的放电顺序写出电极反应式;
解答 解:(1)已知:①N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol
②N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
由盖斯定律可知,①×2-②×2+③×3得:4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-905.0kJ/mol,
17g 氨气的物质的量为:$\frac{17g}{17g/mol}$=1mol,放出的热量Q=1×$\frac{905.0KJ}{4}$=226.3kJ,
故答案为:226.3kJ;
(2)①反应为放热反应,温度升高化学平衡向着吸热方向进行,从T1到T2反应物氮气的量增加,故T1<T2,
故答案为:低于;
②b点代表平衡状态,c点又加入了氢气,故平衡向右移动,氮气的转化率增大,
故答案为:c;
③当氮气和氢气的物质的量之比为1:3时达平衡状态时氨的百分含量最大,平衡点时产物的产率最大,据图示,当平衡时氢气的物质的量为n,故加入N2的物质的量为$\frac{n}{3}$,当n=3mol反应达到平衡时H2的转化率为60%,故起始氮气浓度为1,mol/l,变化的氢气浓度为1.8mol/l,变化的氮气浓度为0.6mol/l,平衡时氮气、氢气、氨气的浓度分别是0.4mol/l、1.2mol/l、1.2mol/l,据K=$\frac{{c}^{2}(N{H}_{3})}{{c}^{3}({H}_{2})c({N}_{2})}$=$\frac{(1.2mol/L)^{2}}{(0.4mol/L)×(1.2mol/L)^{3}}$=2.08 (mol/l)-2,
故答案为:$\frac{n}{3}$;2.08;
(3)①500s,c(N2O5)变化量为5.00-3.52=1.48mol/L,则v(N2O5)=$\frac{△c}{△t}$=$\frac{1.48mol/L}{500s}$=0.00296mol•L-1•s-1,由速率之比等于化学计量数之比可知,v(NO2)=0.00296mol•L-1•s-1×2=0.00592 mol•(L-1•s-1),
故答案为:0.00592 mol•(L-1•s-1);
②燃料原电池中,负极上燃料失电子和碳酸根离子反应生成二氧化碳和水,电极反应式为H2+CO32--2e-=CO2+H2O;
N2O5中氮元素的化合价是+5价,而硝酸中氮元素也是+5价.因此应该在左侧生成N2O5,即在阳极区域生成,据电极反应离子放电顺序可知:阴极发生2H++2e-=H2↑的反应,则阳极为N2O4+2HNO3-2e-=2N2O5+2H+.
故答案为:H2+CO32--2e-=CO2+H2O;N2O4+2HNO3-2e-=2N2O5+2H+.
点评 本题考查了盖斯定律、外界条件对反应速率和平衡的影响、平衡的判断等,题目难度中等,注重高考常考点的考查,注意图象和表格中数据的分析.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:选择题
| A. | 向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度减小 | |
| B. | 由于Ksp(AgCl)>Ksp(AgI),AgCl 沉淀在一定条件下可转化为AgI沉淀 | |
| C. | 在AgCl沉淀溶解平衡体系中加入蒸馏水,AgCl的Ksp增大 | |
| D. | 向等浓度的NaCl和NaI混合溶液中逐滴加入AgNO3溶液,先出现AgI沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

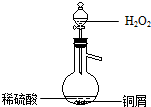 (3)某同学查询资料得知:铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2,铜屑可逐渐溶解.实验小组同学设计实验装置如图,验证该实验,该反应的化学方程式是Cu+H2O2+H2SO4=CuSO4+2H2O.
(3)某同学查询资料得知:铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2,铜屑可逐渐溶解.实验小组同学设计实验装置如图,验证该实验,该反应的化学方程式是Cu+H2O2+H2SO4=CuSO4+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| U | |||
| W | Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:8 | B. | 8:1 | C. | 2:5 | D. | 5:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl晶体、BaSO4 | B. | 铜、二氧化硫 | C. | 硫酸溶液、HCl | D. | 熔融的KNO3、酒精 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com