
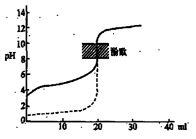
| A����H��0�ķ�Ӧ��������һ�������Է����� |
| B����0.1mol/LNaOH��Һ�ֱ�ζ���ͬ���ʵ���Ũ�Ⱥ���ͬ���������ʹ��ᣬ����ʵ�߱�ʾ���ǵζ���������� |
| C�������£���0.1mol/L��ˮ�У���������NH4Cl���壬��Һ��pH��С |
D�������ܱ������н��еķ�Ӧ3A(g) 2B(g)+C(s)���������������������£��ٳ���һ������A���壬A��ת���ʲ��� 2B(g)+C(s)���������������������£��ٳ���һ������A���壬A��ת���ʲ��� |
 NH4����OH������������NH4Cl���壬����ͬ����ЧӦ��ƽ�����ƣ�OH��Ũ�ȼ�С����Һ��pH��С����ȷ
NH4����OH������������NH4Cl���壬����ͬ����ЧӦ��ƽ�����ƣ�OH��Ũ�ȼ�С����Һ��pH��С����ȷ

 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO2��H2(g) ��Ӧ�����вⶨ�IJ������ݼ��±�������t2��t1��:
CO2��H2(g) ��Ӧ�����вⶨ�IJ������ݼ��±�������t2��t1��:| ��Ӧʱ��/min | n(CO)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(g) +H2(g) ��H= +131.3kJ��mol��1
CO(g) +H2(g) ��H= +131.3kJ��mol��1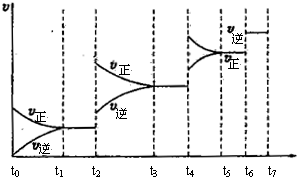
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Z(g)����60s�ﵽƽ�⣬����0.15molZ������˵����ȷ����
Z(g)����60s�ﵽƽ�⣬����0.15molZ������˵����ȷ����| A�������������Ϊ10L��Z��ƽ��Ũ�ȱ�Ϊԭ���Ķ���֮һ |
| B����YŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.0005mol /��L�� s�� |
| C��������ѹǿ��������Y��ת���ʼ�С |
| D���������¶ȣ�X���������������÷�Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3��Ӧ�������б����У�����NH3���������ǣ�
2NH3��Ӧ�������б����У�����NH3���������ǣ�| A��3:1 | B��1:2 | C��2:1 | D��3:8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������


 �����£�Cr(OH)3���ܶȻ�Ksp=10-32����c(Cr3+)����10-5mol/L����Ϊc(Cr3+)�Ѿ���ȫ�������ֽ��ڢ۲���Һ��pHֵ����4����ͨ������˵��Cr3+�Ƿ������ȫ����д��������̣�
�����£�Cr(OH)3���ܶȻ�Ksp=10-32����c(Cr3+)����10-5mol/L����Ϊc(Cr3+)�Ѿ���ȫ�������ֽ��ڢ۲���Һ��pHֵ����4����ͨ������˵��Cr3+�Ƿ������ȫ����д��������̣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 H2��g��+I2��g��������ӦΪ���ȷ�Ӧ��
H2��g��+I2��g��������ӦΪ���ȷ�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 pC(g)+qD(g)����H<0����֪m+n>p+q.����Ӧ��A��B��ɵĻ���↑ʼ,���ֱ�����������´ﵽƽ��:��100��,1��106Paʱ,A��ת����Ϊ��1����200��,1��106Paʱ,A��ת����Ϊ��2����100��,1��107Paʱ,A��ת����Ϊ��3�����1,��2,��3֮��Ĵ�С��ϵ��
pC(g)+qD(g)����H<0����֪m+n>p+q.����Ӧ��A��B��ɵĻ���↑ʼ,���ֱ�����������´ﵽƽ��:��100��,1��106Paʱ,A��ת����Ϊ��1����200��,1��106Paʱ,A��ת����Ϊ��2����100��,1��107Paʱ,A��ת����Ϊ��3�����1,��2,��3֮��Ĵ�С��ϵ��| A����1>��2>��3 | B����3>��2>��1 | C����3 >��1 >��2 | D����1 >��3 >��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com