
����Ŀ����������(ClO2)��һ�ֹ��ס���Ч����������������ˮ��������ˮ�����ȷ����й㷺Ӧ�á�������ijУ��ѧ�о�С�����ʵ����ȡClO2�Ĺ�������ͼ�������й�˵����ȷ����(����)

A.���ʱ������Ӧ�Ļ�ѧ����ʽΪ2HCl![]() Cl2����H2��
Cl2����H2��
B.��NaClO2��Һ��ȡ0.6 mol ClO2ʱ����������0.1 mol NCl3
C.�������Ļ������ͨ��ʢ�м�ʯ�ҵĸ������Գ�ȥClO2�е� NH3
D.��ҺX�ijɷ�ΪNaClO3��NaOH
���𰸡�B
��������
��������ͼ��֪�����ʱ�ķ�Ӧ��ΪNH4Cl��HCl������ΪH2��NCl3�����ݲ����֪��NaClO2��NCl3����������ԭ��Ӧ��ClO2Ϊ�������NH3Ϊ��ԭ�������Ԫ���غ��֪�������ﻹ��NaCl��NaOH�������Ϸ������
A.��������ͼ��֪�����ʱ�ķ�Ӧ��ΪNH4Cl��HCl������ΪH2��NCl3���������ȷ�Ļ�ѧ����ʽΪNH4Cl��2HCl![]() NCl3��3H2����A����
NCl3��3H2����A����
B.NCl3��NaClO2�������ʵ���֮��1:6ǡ�÷�Ӧ����ClO2��NH3��NaCl��NaOH����ϵ����غ��֪��ClԪ�صĻ��ϼ����ߣ���Ԫ�صĻ��ϼ۽��ͣ����ɰ���������ʽΪ��NCl3+6NaClO2+3H2O=6ClO2+3NaCl+3NaOH+NH3����NaClO2��Һ��ȡ0.6 mol ClO2ʱ����������0.1 mol NCl3����B��ȷ��
C.����Ϊ�������壬��ʯ�Ҳ������հ���������ȥNH3��������Ũ�����ȥ��������C����
D.����������ԭ��Ӧ���ɺ�Ԫ���غ��֪����ҺX����Ҫ�ɷ�ΪNaCl��NaOH����D����
�ʴ�ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ��һ����Ҫ�Ļ�������ԭ�ϣ���һ�������¿ɷ�������ת����
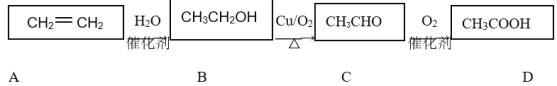
�����������գ�
(1)CH3COOH�Ĺ�����Ϊ________(��ǻ������Ȼ���)��
(2)����ʹ��ˮ��ɫ������ʹ���Ը��������Һ��ɫ����________(�A����B��)��
(3)���B��C�Ļ�ѧ����ʽ��2CH3CH2OH��O2![]() 2CH3CHO��__________��
2CH3CHO��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��һ����Һ̬��(N2H4)Ϊȼ�ϣ�����Ϊ��������ij����������Ϊ����ʵ�����ȼ�ϵ�ء��ù������������ʵĹ����¶ȸߴ�700 -900��ʱ��O2-���ڸù��������������������ƶ�����Ӧ�������Ϊ���������ʡ�����˵����ȷ����

A. �缫������ԭ��Ӧ
B. ����ڵ�O2-�ɵ缫������缫��
C. ����ܷ�ӦΪN2H4 +2O2= 2NO +2H2O
D. ���缫����lmol N2H4����ʱ���ҵ缫����22.4L O2���뷴Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҽ�伮�����������������ű���ķ���������һ�գ���ˮ�����գ���ȡ֭������֮���� ���������Ŷ��з�����ű������Чҩ�����������о����ʾ���á��������ڶԱ�ʵ���з��ֹŷ���Ч���£�����Ƶ���ȡ�����صĹ��տ��Լ��������̣�
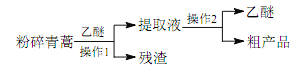
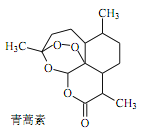
����������Ϣ�����������жϻ������п϶��������
A. ����Ȼֲ������ȡ��Ч�ɷ����Ƽ�����ҩ���з�����Ҫ;��
B. �����������������Ч�ɷֵ���ȡ��
C. ������������ˮ������
D. ���� 1 �ǹ��ˣ����� 2 ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. �����������£�CH3CO18OC2H5��ˮ�������CH3COOH �� C2H518OH
B. ��ȩ�ͱ�ϩȩ����ͬϵ�������H2 ��ַ�Ӧ��IJ�����ͬϵ��
C. �ױ���ʹ���Ը��������Һ��ɫ�������˲����Ա�����Ӱ��
D. ���ᱡ�ɴ���(![]() )�ܷ���ˮ�ⷴӦ��������Ӧ����ȥ��Ӧ��ȡ����Ӧ
)�ܷ���ˮ�ⷴӦ��������Ӧ����ȥ��Ӧ��ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������ϡ���![]() �Ͻ���Cr�����仯�ĸ�ʴ��ʵ�����������й�˵����ȷ����
�Ͻ���Cr�����仯�ĸ�ʴ��ʵ�����������й�˵����ȷ����
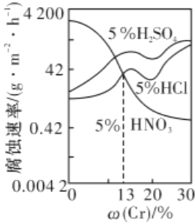
A.ϡ�����![]() �Ͻ�ĸ�ʴ�Ա�ϡ�����ϡ�������
�Ͻ�ĸ�ʴ�Ա�ϡ�����ϡ�������
B.ϡ���������Ӧ�Ļ�ѧ����ʽ�ǣ�Fe+6HNO3(ϡ)![]() Fe��NO3��3+3NO2��+3H2O
Fe��NO3��3+3NO2��+3H2O
C.Cr��������13%ʱ����Ϊ�������������������Ũ��������Զ�![]() �Ͻ�ĸ�ʴ����ǿ
�Ͻ�ĸ�ʴ����ǿ
D.����Cr�������ӣ�ϡ�����![]() �Ͻ�ĸ�ʴ�Լ���
�Ͻ�ĸ�ʴ�Լ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��¡����ݵ��ܱ������н��з�Ӧ A��g���TB��g��+C��g��������Ӧ���Ũ����2molL-1 ���� 0.8molL-1 ��Ҫ 20s����ô��Ӧ��Ũ������ 0.8molL-1 ���� 0.2molL-1 ����Ҫ��ʱ��Ϊ
A.10sB.���� 10sC.С�� 10sD.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij̼�ظֹ�¯��ˮ������Ҫ�ɷ���̼��ơ�����ơ�������þ�����⡢��������ȡ�ˮ�����γɰ�ȫ�������輰ʱ��ϴ��ȥ����ϴ�������£�
����NaOH��Na2CO3���Һ�����ȣ�������Сʱ��
�ų�ϴ�ӷ�Һ����ˮ��ϴ��¯������ϡ���������NaF��Һ�����ݣ�
����ϴҺ�м���Na2SO3��Һ��
������ϴ��꣬��NaNO2��Һ�ۻ���¯��
��1����NaOH�ܽ��������Ļ�ѧ����ʽ��__________________________________��
��2����֪��20��ʱ�ܽ��/g
CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
1.4��10-3 | 2.55��10-2 | 9��10-4 | 1.1��10-2 |
�������ݣ���ϻ�ѧƽ��ԭ��������ϴCaSO4�Ĺ���________________________��
��3���ڲ�����У�
�� ��������ˮ���������⣬����_______________________________________��
�� ��ϴ�����У��ܽ���������ٹ�¯��ʴ�������ӷ���ʽ������ԭ��________��
��4��������У�����Na2SO3��Ŀ����_______________________��
��5��������У��ۻ���Ĺ�¯����Ḳ��һ�����ܵ�Fe2O3����Ĥ��
�� ��ɲ���ƽ�䷴Ӧ�����ӷ���ʽ��______
![]()
��������ۻ�Ч���ķ�����������______��
a����¯���ϵμ�ŨH2SO4���۲���Һ�����ػ�ɫ��ʱ��
b����¯���ϵμ�����CuSO4��Һ���۲���ɫ��ʧ��ʱ��
c����¯���ϵμ�����K3[Fe(CN)6]��Һ���۲������ɫ������ʱ��
d����¯���ϵμ�ŨHNO3���۲���ֺ���ɫ�����ʱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
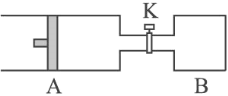
����Ŀ����ͼ��ʾ��A�г���1 mol X ��1 mol Y����B�г���2 mol X��2 mol Y����ʼʱ��
V(A) = V(B) = a L������ͬ�¶Ⱥ��д��������£��������и��Է���������Ӧ��X(g)+Y(g)![]() 2Z(g)+W(g) ��H��0���ﵽƽ��ʱ��V(A) = 1.1a L������ͨ��������������ƣ�����˵����ȷ����(����)
2Z(g)+W(g) ��H��0���ﵽƽ��ʱ��V(A) = 1.1a L������ͨ��������������ƣ�����˵����ȷ����(����)
A. n(Z)B = 2n(Z)A
B. A������X��ת����Ϊ20%
C. ����A��B�о��ټ���1molX��1molY��X���������������
D. ��K�����¶Ȳ��䣬�ִﵽƽ��ʱ��A�����Ϊ3.3a L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com