
[化学一选修2:化学与技术](15分)已知:
①工业上用硫酸与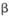 -锂辉矿(LiAlSi2O6和少量钙镁杂质)反应,生成Li2SO4、MgSO4 等,最终制备金属锂。
-锂辉矿(LiAlSi2O6和少量钙镁杂质)反应,生成Li2SO4、MgSO4 等,最终制备金属锂。
②氢氧化锂在一定温度下可转化为氧化锂。
用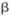 -锂辉矿与硫酸等物质制备金属锂的工业流程如下图:
-锂辉矿与硫酸等物质制备金属锂的工业流程如下图:

请回答:
(1)沉淀Y的主要成分的化学式是____________。
(2)流程中使用了不同浓度的Na2CO3溶液,从物质溶解度大小的角度解释其使用的原因____________
(3 )操作1涉及的实验方法是__________________。
(4 )写出用铝粉还原法制取金属锂的化学反应方程式。________________________
(5) LiCl溶液加热蒸干后,所得固体在熔融状态下电解制备锂。电解时产生的氯气中混 有少量氧气,产生氧气的原因是__________________
(6) 目前电池通常使用金属锂的优点是__________________
(1) Li2CO3(2分)
(2) CaCO3 的溶解度小于Li2CO3,加稀Na2CO3溶液既能除去溶液中的Ca2+,又不生成Li2CO3沉淀;(2分) 加饱和Na2CO3溶液的目的是使Li +转化生成Li2CO3沉淀。(2分)
(3) 过滤 洗涤(2分) (4)2Al+3Li2O 6Li + Al2O3 (2分)
6Li + Al2O3 (2分)
(5)LiCl溶液在加热蒸干过程中有部分LiOH生成,LiOH受热分解为Li2O,熔融的Li2O电解生成氧气。(3分)
(6)锂的质量轻,负电位高、比能量高;锂电池为可充电绿色环保电池。(2分,其它合理答案也给分)
【解析】本题以工业制锂为载体考查了沉淀溶解平衡,水解、原电池和电解等相关原理
(1)硫酸锂和碳酸钠饱和溶液反应,生成碳酸锂沉淀和硫酸钠,根据Y灼烧的产物是氧化锂可知, Y是碳酸锂。
(2)X是氢氧化镁和碳酸钙沉淀,由于CaCO3 的溶解度小于Li2CO3,加稀Na2CO3溶液既能除去溶液中的Ca2+,又不生成Li2CO3沉淀;而后来加饱和Na2CO3溶液的目的是使Li +转化生成Li2CO3沉淀。
(3)从溶液中分离出固体的方法应是过滤,过滤后晶体必须洗涤。
(4)在加热的条件下,铝可以发生铝热反应,方程式为2Al+3Li2O 6Li
+ Al2O3。
6Li
+ Al2O3。
(5)混有O2的原因必须从反应物特征入手寻找,由于加热蒸干LiCl溶液可获得固体,但是由于LiCl受热易水解成LiOH,LiOH受热分解产生的Li2O电解时会产生O2。
(6)锂的质量轻,负电位高、比能量高,且锂电池为可充电绿色环保电池。


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:阅读理解
|
压强/MPa SO2转化率 温度/℃ |
0.1 |
0.5 |
1 |
10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
| ||
| △ |
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012届河北省冀州市中学高三联排考试化学试卷(带解析) 题型:填空题
【化学一选修2化学与技术】(15分)
已知:①工业上用硫酸与锂辉矿(LiA1Si2O6和少量钙镁杂质)反应,生成Li2SO4、MgSO4等,最终制备金属锂。
②氢氧化锂在一定温度下可转化为氧化锂。用β锂辉矿与硫酸等物质制备金属锂的工业流程如下: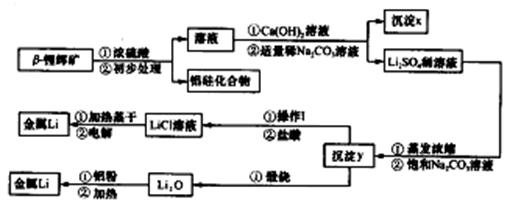
请回答:(1)沉淀y的主要成分的化学式是 。
(2)流程中使用了不同浓度的Na2CO3溶液,从物质溶解度大小的角度解释其浓度不同的原因是 。
(3)操作I涉及的实验方法是 。
(4)写出用铝粉还原法制取金属锂的化学方程式 。
(5)LiCl溶液加热蒸干后,所得固体在熔融状态下电解制备锂。电解时产生的氯气中混有少量氧气,产生氧气的原因是 。
(6)目前电池通常使用金属锂的优点是 。
查看答案和解析>>
科目:高中化学 来源:2012届河北省石家庄市高三第二次模拟理科综合化学试卷(带解析) 题型:填空题
[化学一选修2:化学与技术](15分)已知:
①工业上用硫酸与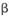 -锂辉矿(LiAlSi2O6和少量钙镁杂质)反应,生成Li2SO4、MgSO4等,最终制备金属锂。
-锂辉矿(LiAlSi2O6和少量钙镁杂质)反应,生成Li2SO4、MgSO4等,最终制备金属锂。
②氢氧化锂在一定温度下可转化为氧化锂。用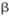 -锂辉矿与硫酸等物质制备金属锂的工业流程如下图:
-锂辉矿与硫酸等物质制备金属锂的工业流程如下图: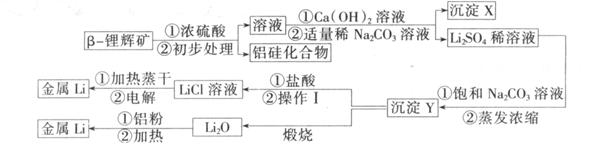
请回答:
(1)沉淀Y的主要成分的化学式是____________。
(2)流程中使用了不同浓度的Na2CO3溶液,从物质溶解度大小的角度解释其使用的原因____________
(3 )操作1涉及的实验方法是__________________。
(4 )写出用铝粉还原法制取金属锂的化学反应方程式。________________________
(5) LiCl溶液加热蒸干后,所得固体在熔融状态下电解制备锂。电解时产生的氯气中混有少量氧气,产生氧气的原因是__________________
(6) 目前电池通常使用金属锂的优点是__________________
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河北省冀州市高三联排考试化学试卷(解析版) 题型:填空题
【化学一选修2化学与技术】(15分)
已知:①工业上用硫酸与锂辉矿(LiA1Si2O6和少量钙镁杂质)反应,生成Li2SO4、MgSO4等,最终制备金属锂。
②氢氧化锂在一定温度下可转化为氧化锂。用β锂辉矿与硫酸等物质制备金属锂的工业流程如下:
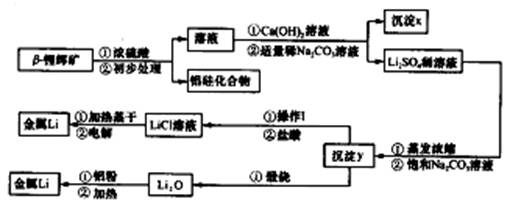
请回答:(1)沉淀y的主要成分的化学式是 。
(2)流程中使用了不同浓度的Na2CO3溶液,从物质溶解度大小的角度解释其浓度不同的原因是 。
(3)操作I涉及的实验方法是 。
(4)写出用铝粉还原法制取金属锂的化学方程式 。
(5)LiCl溶液加热蒸干后,所得固体在熔融状态下电解制备锂。电解时产生的氯气中混有少量氧气,产生氧气的原因是 。
(6)目前电池通常使用金属锂的优点是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com