

 Ҳ����������Ʒ�Ӧ�۵ķ�Ӧ�����л���V��V�Ľṹ��ʽ��
Ҳ����������Ʒ�Ӧ�۵ķ�Ӧ�����л���V��V�Ľṹ��ʽ��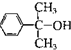 �����ȡ����Ӧ��������ԭ�ӱ�
�����ȡ����Ӧ��������ԭ�ӱ� ȡ����
ȡ����| ˮ |
| �� |
| ˮ |
| �� |
 ��
�� ��
��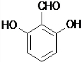 ��
�� ��
�� ��
�� ����дһ�֣���
����дһ�֣��� ����ԭ�ӱ�
����ԭ�ӱ� ȡ������V�Ľṹ��ʽΪ��
ȡ������V�Ľṹ��ʽΪ��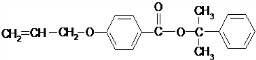 ��
�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��FeCl3��Һ��Cu�ķ�Ӧ��Cu+Fe3+=Cu2++Fe2+ | ||||
| B��NO2��ˮ�ķ�Ӧ��3NO2+H2O=2NO3-+2H++NO | ||||
| C��������Һ��ˮ���е�CaCO3��Ӧ��CaCO3+2H+=Ca2++H2O+CO2�� | ||||
D���ò��缫����Ȼ�þ��Һ��2Cl-+2H2O
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| NBS |
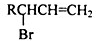
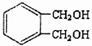 ��ͬ���칹����ͬʱ�������������ķ����廯���ﹲ��
��ͬ���칹����ͬʱ�������������ķ����廯���ﹲ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������Ƭ�ʹ���Ƭ����ͼ��ʽ����ͬŨ�ȵ�NaOH��Һ��һ��ʱ�䣬����������ȷ���ǣ�
������Ƭ�ʹ���Ƭ����ͼ��ʽ����ͬŨ�ȵ�NaOH��Һ��һ��ʱ�䣬����������ȷ���ǣ�| A�����ձ�����Ƭ����������ݲ��� |
| B��������Ƭ��������������Ƭ�Ǹ��� |
| C�����ձ�����Һ��pH������ |
| D���������ݵ��ٶȼױ��ҿ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ܣ���=�ڣ��� |
| B���ܣ���=�ڣ��� |
| C���٣��ڣ��ۣ��� |
| D���ܣ��ۣ��ڣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ȷ�����ǣ�
����ȷ�����ǣ�| A��2��5-����-4-�һ����� |
| B��2��5-����-3-�һ����� |
| C��3-�����-5-������ |
| D��2-��-4-��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �ⶨ��� | ������Һ�������mL�� | ���������Һ�������mL�� | |
| �ζ�ǰ���� | �ζ������ | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com