
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是
①中实验②中现象()
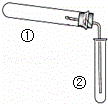
A. 铁粉与水蒸气加热 肥皂水冒泡
B. 加热NH4Cl和Ca(OH)2混合物 酚酞溶液变红
C. NaHCO3固体受热分解 澄清石灰水变浑浊
D. 石蜡油在碎瓷片上受热分解 Br2的CCl4溶液褪色
考点: 实验装置综合.
专题: 实验评价题.
分析: A.试管中空气受热碰撞;
B.加热NH4Cl和Ca(OH)2混合物,生成氨气,其水溶液显碱性;
C.NaHCO3固体受热分解生成二氧化碳;
D.石蜡油在碎瓷片上受热分解生成乙烯,可发生加成反应.
解答: 解:A.试管中空气受热碰撞,则②中肥皂水冒泡可能与试管中空气有关,不能说明氢气的生成,故A选;
B.加热NH4Cl和Ca(OH)2混合物,生成氨气,其水溶液显碱性,则酚酞溶液变红可说明反应的发生,故B不选;
C.NaHCO3固体受热分解生成二氧化碳,则澄清石灰水变浑浊可说明反应的发生,故C不选;
D.石蜡油在碎瓷片上受热分解生成乙烯,可发生加成反应,则Br2的CCl4溶液褪色可说明反应的发生,故D不选;
故选A.
点评: 本题考查实验装置的综合,为高频考点,把握图中装置的作用及发生的反应、物质的性质为解答的关键,侧重分析、实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:
下列各组性质比较中,正确的是( )
①酸性:HClO4>HBrO4>HIO4
②离子还原性:S2﹣>Cl﹣>Br﹣>I﹣
③沸点:HF>HCl>HBr>HI
④金属性:K>Na>Mg>Al
⑤气态氢化物稳定性:HF>HCl>H2S
⑥半径:O2﹣>Na+>Na>Cl.
A. ①②③ B. ②③④ C. ①④⑤ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式:
①H2(g)+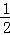 O2(g)═H2O(g);△H=﹣241.8kJ•mol﹣1
O2(g)═H2O(g);△H=﹣241.8kJ•mol﹣1
②2H2(g)+O2(g)═2H2O(g);△H=﹣483.6kJ•mol﹣1
③H2(g)+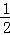 O2(g)═H2O(l);△H=﹣285.8kJ•mol﹣1
O2(g)═H2O(l);△H=﹣285.8kJ•mol﹣1
④2H2(g)+O2(g)═2H2O(l);△H=﹣571.6kJ•mol﹣1则氢气的燃烧热为()
A. 241.8 kJ•mol﹣1 B. 483.6 kJ•mol﹣1
C. 285.8 kJ•mol﹣1 D. 571.6 kJ•mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应2A(g)⇌B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
实验
序号 时间
浓度
温度 0 10 20 30 40 50 60
1 800℃ 1.0 0.80 0.67 0.57 0.50 0.50 0.50
2 800℃ c2 0.60 0.50 0.50 0.50 0.50 0.50
3 800℃ c3 0.92 0.75 0.63 0.60 0.60 0.60
4 820℃ 1.0 0.40 0.25 0.20 0.20 0.20 0.20
根据上述数据,完成下列填空:
(1)在实验1,反应在20至30分钟时间内用A表示表示该反应的平均速率为
(2)在实验2,A的初始浓度c2=1.0mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填“<”、“=”或“>”),且c3 0mol/L(填“<”、“=”或“>”).
(4)比较实验4和实验1,可推测该反应是 (选填吸热、放热).理由是
查看答案和解析>>
科目:高中化学 来源: 题型:
以石墨为电极,电解含有少量酚酞和淀粉的NaI溶液.已知:通常条件下,I﹣的放电能力比Cl﹣更强.下列说法错误的是()
A. 阴极附近溶液呈红色 B. 阴极逸出气体
C. 阳极附近溶液呈蓝色 D. 溶液的pH变小
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨是人类科学技术上的一项重大突破,其反应原理为:N2(g)+3H2(g)⇌2NH3(g)+Q(Q>0)
一种工业合成氨的简易流程图如下:
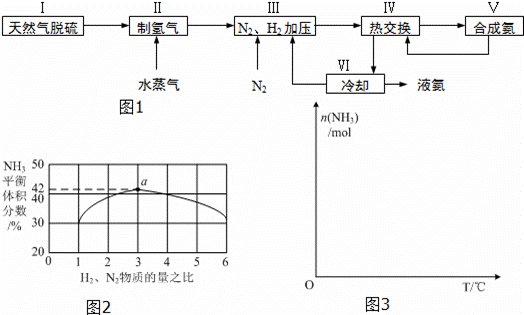
完成下列填空:
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS.一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生.NH4HS的电子式是 ,写出再生反应的化学方程式: .NH3的沸点高于H2S,是因为NH3分子之间存在着一种比 更强的作用力.
(2)室温下,0.1mol/L的氯化铵溶液和0.1mol/L的硫酸氢铵溶液,酸性更强的是 .已知:H2SO4:Ki2=1.2×10﹣2NH3•H2O:Ki=1.8×10﹣5.
(3)图2表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系.根据图中a点数据计算N2的平衡体积分数: (答案用小数表示,保留3位有效数字).
(4)依据温度对合成氨反应的影响,在图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图.
(5)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号) .简述本流程中提高合成氨原料总转化率的方法: .
查看答案和解析>>
科目:高中化学 来源: 题型:
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
|
| A. | 未通电前上述镀锌装置可构成原电池,锌为负极,电镀时锌与电源负极相连为阴极 |
|
| B. | 电镀时通过1mol电子,阴极上有0.5mol锌的析出 |
|
| C. | 未通电前K+向铁极移动,通电后K+还向铁极移动 |
|
| D. | 镀锌层破损后对铁制品失去保护作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列说法正确的是( )
|
| A. | 2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
|
| B. | 32g氧气所含原子数目为NA |
|
| C. | 17g氨气所含电子数目为10NA |
|
| D. | 1.8g水所含的质子数目为10NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com