
分析 气态烃在标准状况下的密度为1.34g/L,则摩尔质量为1.34g/L×22.4K/mol=30g/mol,现取一定质量该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰中,浓硫酸增重13.5g,则n(H2O)=$\frac{13.5g}{18g/mol}$=0.75mol,碱石灰增重22g,则n(CO2)=$\frac{22g}{44g/mol}$=0.5mol,可确定C原子、H原子的个数比,即求出的实验式,再结合烃的相对分子质量确定其分子式.
解答 解:(1)气态烃在标准状况下的密度为1.34g/L,则摩尔质量为1.34g/L×22.4K/mol=30g/mol,则相对分子质量为30,故答案为:30;
(2)现取一定质量该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰中,浓硫酸增重13.5g,则n(H2O)=$\frac{13.5g}{18g/mol}$=0.75mol,碱石灰增重22g,则n(CO2)=$\frac{22g}{44g/mol}$=0.5mol,则C原子、H原子的个数比为0.5:.075×2=1:3,实验式为CH3,相对分子质量为30,则分子式为C2H6,
故答案为:CH3;C2H6.
点评 本题考查有机物分子式的确定,为高频考点,侧重于学生的分析能力和计算能力的考查,题目难度中等,注意掌握常见的有机物分子式的确定方法,明确根据质量守恒定律确定有机物的分子式的方法.


科目:高中化学 来源: 题型:实验题
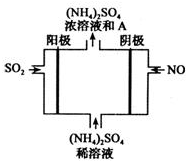 经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.
经研究发现,含pM2.5的雾霾主要成分有SO2、NOx、CxHy,及可吸入颗粒等.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
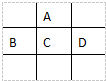 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某电中性单核粒子含有6个电子、7个中子,该粒子是${\;}_{6}^{13}$C | |
| B. | 在Na+、O2-、Cl、Cl-四种粒子中,半径最大的是Cl-,半径最小的是Na+ | |
| C. | 在离子RO3n-中共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是A-x+n+24 | |
| D. | 硫离子的结构示意图为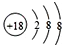 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
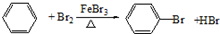 反应类型取代反应.
反应类型取代反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com