
 ij�¶�ʱ����2L�ܱ������У�������̬����X��Y��Z�����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ����ɵã�
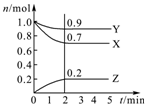
ij�¶�ʱ����2L�ܱ������У�������̬����X��Y��Z�����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ����ɵã����� ��1������ͼ��֪�����ŷ�Ӧ���У�X��Y�����ʵ������ٶ�Z���ʵ�������˵��X��Y�Ƿ�Ӧ���Z��������������ʵ����ı仯�жϷ�Ӧ���������������ʵ����ı仯֮�ȵ��ڻ�ѧ������֮����д����ʽ��ת����=$\frac{ת����}{��ʼ��}$��100%���㣻
��2��������������Ի�ѧ��Ӧ���ʵ�Ӱ�����ؿ�֪�������¶ȡ�����ѹǿ��ʹ�ô����ȶ�����ʹ��Ӧ��������֮���С��Ӧ���ʣ��ݴ��жϣ�
��� �⣺��1������ͼ��֪�����ŷ�Ӧ���У�X��Y�����ʵ������ٶ�Z���ʵ�������˵��X��Y�Ƿ�Ӧ���Z���������ͼ����Կ�������Ӧ��X��Y�����ʵ�����С��Z�����ʵ������࣬��X��YΪ��Ӧ�ZΪ������ҡ�n��X������n��Y������n��Z��=0.1mol��0.3mol��0.2mol=1��3��2����Ӧ�Ļ�ѧ����ʽΪ3X+Y?2Z
����ͼ����֪X��ƽ���1mol��Ϊ0.7mol����ת����=$\frac{1mol-0.7mol}{1mol}$��100%=30%��
�ʴ�Ϊ��3X+Y?2Z��30%��
��2��������������Ի�ѧ��Ӧ���ʵ�Ӱ�����ؿ�֪�������¶ȡ�����ѹǿ��ʹ�ô����ȶ�����ʹ��Ӧ��������֮���С��Ӧ���ʣ�
�ٽ����¶����С��Ӧ���ʣ��ʢٴ���
�ڼ��������������䣬��Ӧ���Ũ�Ȳ��䣬���Է�Ӧ���ʲ��䣬�ʢڴ���
�ۼ����������Ӧ���ʣ��ʢ���ȷ��
�ܱ���������������䣬����A��g�������ʵ���������Ӧ��Ũ�ȣ�������Ӧ���ʣ��ʢ���ȷ��
�ʴ�Ϊ���ۢܣ�
���� ���⿼�黯ѧƽ��ͼ���������Ӧ���ʼ��㡢Ӱ�췴Ӧ�������أ���Ŀ�ѶȲ���ע����������ʵ����ı仯���ߣ����ջ�ѧ����ʽ���жϷ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | K+ 1s22s22p63s23p6 | B�� | F 1s22s22p5 | ||
| C�� | S2- 1s22s22p63s23p4 | D�� | Ar 1s22s22p63s23p6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ά�ؾ����ڸ߷��ӻ����� | |
| B�� | ��ͬ����֬����������Ӧ��������һ�ֲ�����ͬ | |
| C�� | ������ϡ���������³�ּ��Ⱥ�������Һ����������Cu��OH��2����δ����ɫ������˵������δ����ˮ�� | |
| D�� | ��������Һ�м���ƾ���ᷢ��������ʧȥ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 5�ֹ�������A��B��C��D��E�ɱ��в�ͬ������������ɣ����Ǿ�������ˮ��
5�ֹ�������A��B��C��D��E�ɱ��в�ͬ������������ɣ����Ǿ�������ˮ��| ������ | Na+�� Al3+Fe3+�� Cu2+��Ba2+ |
| ������ | OH-��Cl-��CO32-��NO3-��SO4- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCO3-ˮ������ӷ���ʽ��HCO3-+H2O?CO32-+H3O+ | |
| B�� | ��ˮ��ͨ��������SO2��I2+SO2+2H2O�T2I-+SO42-+4H+ | |
| C�� | ������SO2ͨ��NaOH��Һ�У�SO2-+2OH-=SO32-+H2O | |
| D�� | ��������Һ�еμӹ�����ˮ��Ag++NH3•H2O�TAgOH��+NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | -332kJ | B�� | -118kJ | C�� | +130kJ•mol-1 | D�� | +350kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
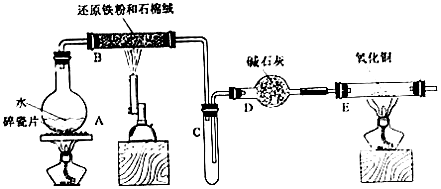
| ���� | ���� | �������� | �������� | |
| 1 | ȡ��ɫ��ĩ����ϡ���� | ��⣬������ | �ܽ⣬������ | |
| 2 | ȡ����1����Һ���μ�����KMnO4��Һ | ��ɫ��ȥ | ��ɫ��ȥ | |
| 3 | ȡ����1����Һ���μ�KSCN��Һ | ��� | ������ | |
| 4 | ����3��Һ�еμ�������ˮ | ��ɫ��ȥ | �ȱ�죬����ɫ | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
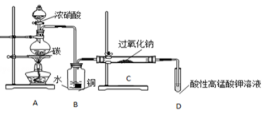 �������ƣ�NaNO2����һ�ֳ�����ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������ij��ȤС���������ʵ��̽������������֪����
�������ƣ�NaNO2����һ�ֳ�����ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������ij��ȤС���������ʵ��̽������������֪����| �ζ����� | 1 | 2 | 3 | 4 |
| KMnO4��Һ���/mL | 20.60 | 20.02 | 20.00 | 19.98 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com