
【题目】已知:(HF)2(g) ![]() 2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
2HF(g) △H>0,平衡体系的总质量m(总)与总物质的量n(总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
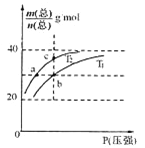
A.温度:T1< T2
B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:v(b)>v(a)
D.当![]() 30g·mol-1时,n(HF):n[(HF)2]=2:1
30g·mol-1时,n(HF):n[(HF)2]=2:1
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】有机物的反应往往伴随副反应发生,因此 需要分离提纯。有一种水果香精的合成步骤如下:
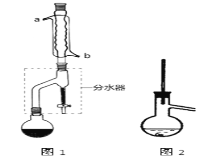
Ⅰ合成:
在干燥的圆底烧瓶中加入11.5 mL(9.3 g,0.125 mol)正丁醇、7.2 mL(7.5 g,0.125 mol)冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再按图1所示装置安装好。在分水器中预先加入5.00 mL水,其水面低于分水器回流支管下沿3~5 mm,然后用小火加热,反应大约40 min。
Ⅱ分离提纯:
① 将烧瓶中反应后的混合物冷却后与分水器中的酯层合并,转入分液漏斗,依次用10 mL水、10 mL 10% 碳酸钠溶液洗至中性,充分振荡后静置,分去水层。
② 将酯层倒入小锥形瓶中,加少量无水硫酸镁干燥。
③ 将乙酸正丁酯粗产品转入50 mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品。
主要试剂及产物的物理常数如下:
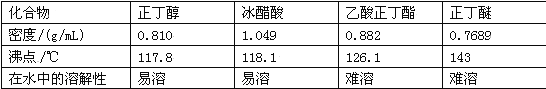
制备过程中还可能有的副反应:
2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
(1)合成和分离过程中均使用沸石,其作用________________________ 。
(2)如图1整个装置可看作由分水器、圆底烧瓶和冷凝管组成,其中冷水应从______(填a或b)管口通入。
(3)在操作步骤②后(即酯层用无水硫酸镁干燥后),应先_______(填实验操作名称),然后将乙酸正丁酯粗产品转入蒸馏烧瓶中,如果蒸馏装置如图2所示,则收集到的产品中可能混有___________杂质。
(4)步骤③的常压蒸馏,需控制一定的温度,你认为在______中加热比较合适(请从下列选项中选择)。
A.水 B.甘油(沸点290℃)
C.沙子 D.石蜡油(沸点200~300℃)
(5)如何根据装置中的实验现象判断该合成反应达到了终点_______________ 。
(6)反应结束后,若放出的水为6.98 mL(水的密度为1g/mL),则正丁醇的利用率约为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源。下图是从海水中提取某些原料的流程图。

下列有关说法正确的是( )
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.工业上通过氯碱工业制取金属钠
C.从第③步到第⑤步的目的是浓缩、富集溴单质
D.第②步的反应条件是高温加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取COC2O4·2H2O工艺流程如下:
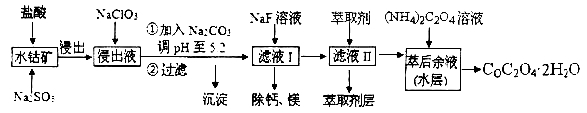
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:

(1)浸出过程中加入Na2SO3的目的是_______________。
(2)NaClO3在反应中氯元素被还原为最低价,该反应的离子方程式为 ______________。
(3)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀。试用离子方程式和必要的文字简述其原理:_____________________________________。
(4)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液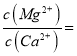 ______。
______。
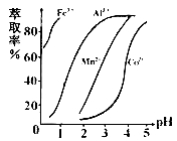
(5)萃取剂对金属离子的萃取率与pH的关系如右图所示,在滤液II中适宜萃取的pH为___左右。
a.1 b.2 c.3 d.4
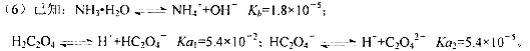
则该流程中所用(NH4)2C2O4溶液的pH_____7(填“>”或“<”或“=”)
(7)CoC2O4·2H2O热分解质量变化过程如右图所示(其中600℃以前是隔绝空气加热,600℃以后是在空气中加热);A、B、C均为纯净物;C点所示产物的化学式是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg/L,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg/L。某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO。

1、测定原理:
碱性条件下,O2将Mn2+氧化为MnO(OH)2:①2Mn2++O2+4OH="2" MnO(OH)2↓
酸性条件下,MnO(OH)2将I氧化为I2:②MnO(OH)2+I+H+→Mn2++I2+H2O(未配平),用Na2S2O3标准溶液滴定生成的I2:③2S2O32+I2=S4O62+2I
2、测定步骤
a.安装装置,检验气密性,充N2排尽空气后,停止充N2。
b.向烧瓶中加入200mL水样。
c.向烧瓶中依次迅速加入1mLMnSO4无氧溶液(过量)、2mL碱性KI无氧溶液(过量),开启搅拌器,至反应①完全。
d搅拌并向烧瓶中加入2mL硫酸无氧溶液至反应②完全,溶液为中性或弱酸性。
e.从烧瓶中取出40.00mL溶液,以淀粉作指示剂,用0.01000mol/L Na2S2O3溶液进行滴定,记录数据。
f.……
g.处理数据(忽略氧气从水样中的逸出量和加入试剂后水样体积的变化)。
回答下列问题:
(1)配置以上无氧溶液时,除去所用溶剂水中氧的简单操作为__________。
(2)在橡胶塞处加入水样及有关试剂应选择的仪器为__________。
①滴定管②注射器③量筒
(3)搅拌的作用是__________。
(4)配平反应②的方程式,其化学计量数依次为__________。
(5)步骤f为__________。
(6)步骤e中达到滴定终点的标志为__________。若某次滴定消耗Na2S2O3溶液4.50mL,水样的DO=__________mg/L(保留一位小数)。作为饮用水源,此次测得DO是否达标:__________(填“是”或“否”)
(7)步骤d中加入硫酸溶液反应后,若溶液pH过低,滴定时会产生明显的误差,写出产生此误差的原因(用离子方程式表示,至少写出2个)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
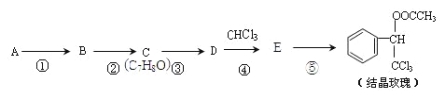
【题目】结晶玫瑰是具有玫瑰香气的香料,可由下列方法合成(部分反应物及反应条件未标出)
已知: ![]() (-R表示烃基)
(-R表示烃基)
(1)A是苯的一种同系物,相同条件下,其蒸气对氢气的相对密度是46,则A的结构简式是 。
(2)反应①的条件是氯气和光照,则反应②的方程式是 。
(3)D的核磁共振氢谱共有 组峰。
(4)③的化学方程式是 。
(5)C有多种同分异构体,写出其中含苯环且不属于酚类的同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成治疗高血压药物奈必洛尔的重要中间体,其部分合成路线图如下(Ph代表苯基):
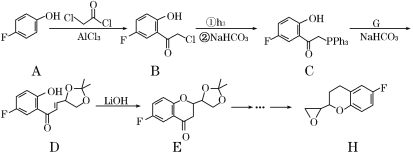
(1)化合物C的含氧官能团名称为________、________。
(2)B→C的反应类型是________。
(3)写出A→B的化学反应方程式________。
(4)C→D的转化中,反应物G的分子式为C6H10O3,生成物除D外还有Ph3P=O,则G的结构简式为_________
(5)写出同时满足下列条件的B的一种同分异构体的结构简式________。
Ⅰ.分子中含有一个酯基和一个手性碳原子,有4种化学环境不同的氢;
Ⅱ.不能发生银镜反应;
Ⅲ.能发生水解反应,且其中一种水解产物能与FeCl3溶液发生显色反应。
(6)已知:
①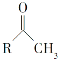
![]() RCOONa
RCOONa
②![]()
![]()
![]()
化合物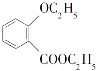 是一种重要的有机合成中间体,请写出以苯酚、乙醇和
是一种重要的有机合成中间体,请写出以苯酚、乙醇和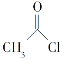 为原料制备该化合物的合成路线流程图(无机试剂作用)。合成路线流程图示例如下:
为原料制备该化合物的合成路线流程图(无机试剂作用)。合成路线流程图示例如下:
H2C===CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳单质及其化合物有广泛的应用。
(1)碳的同素异性体金刚石、石墨和C60晶体中,能溶于有机溶剂的是___,原因是_______。
(2)CH3COCH=CHCH3分子中,C原子所采取的杂化类型有____________。
(3)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图所示,图中用虚线标出了石墨的一个六方晶胞。该晶胞中含有的碳原子数为_____个。
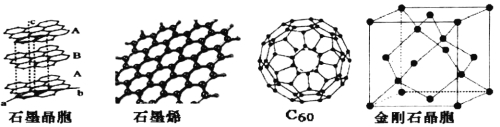
(4)石墨烯是一种由单层碳原子构成的平面结构新型碳材料,如图所示。1mol石墨烯中含有的六元环个数为______,下列有关石墨烯说法正确的是________
a.晶体中碳原子间全部是碳碳单键
b.石墨烯中所有碳原子可以处于同一个平面
c.从石墨中剥离得到石墨烯需克服分子间作用力
(5)石墨烯可转化为C60,C60的结构如图所示,该分子是由五边形和六边形构成的球体,其中五边形有12个,六边形有________个。
(6)金刚石晶胞如图所示,则金刚石晶胞中原子的配位数为_____,原子空间利用率为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙烯为原料合成环状化合物 E(C4H4O4)的流程如下。
![]()
请回答下列问题:
(1)E 的结构简式是_______________;C 中所含官能团的名称是____________。
(2)在乙烯的同系物中,所有碳原子一定共平面且碳原子数最多的分子的结构简式是__________,名称(系统命名)是______________。
(3)反应①⑤中,属于取代反应的是_______(填写编号)。
(4)写出反应②的化学方程式______________ 。
(5)F是E的同分异构体,且1 mol F与足量的 NaHCO3溶液反应可放出2mol CO2气体,请写出符合条件的F的所有的结构简式______________ 。
(6)参照上述合成路线的表示,设计以乙烯为原料制备乙二醇的最简合成路线:
__________________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com