
【题目】能区分胶体和溶液的方法是
A.静置,有沉淀现象的是胶体B.能透过滤纸的是溶液
C.有丁达尔现象的是胶体D.用肉眼观察,均匀透明的是溶液
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)某温度下,在体积为5 L的容器中,A、B、C三种物质物质的量随着时间变化的关系如图所示,则该反应的化学方程式为__________,2 s内用A的浓度变化和用B的浓度变化表示的平均反应速率分别为________、________。

(2)把0.6 mol X气体与0.6 mol Y气体混合于2 L容器中发生反应:2X(g)+Y(g)=nZ(g)+2W(g),2 min末已生成0.2 mol W,若测得以v(Z)浓度变化表示的v(Z)=0.1 mol/(L·min)。求:
(1)n=_____?
(2)前2 min内,v(X)=_____?
(3)2 min末时Y的浓度_____?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硫的说法不正确的是( )
A.单质硫既有氧化性,又有还原性B.硫在空气中的燃烧产物是二氧化硫
C.铜与硫反应生成黑色的硫化铜D.硫与氢气反应的氧化剂是硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物丙可由如下反应得到:![]()
![]()
![]()
![]()
![]() 。丙的结构简式不可能是
。丙的结构简式不可能是
A. CH3CH(CH2Br)2 B. (CH3)2CBrCH2Br
C. CH3CH2CHBrCH2Br D. CH3CHBrCHBrCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定体积0.1mol/L醋酸溶液中加入等体积的蒸馏水后,则下列叙述正确的是( )
A.溶液的pH值变小
B.醋酸的电离程度降低
C.溶液的导电能力减弱
D.中和此溶液所需的0.1mol/LNaOH溶液的体积增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积2L的密闭容器中加入反应物N2、H2,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。反应过程中的部分数据如下表所示,下列说法正确的是
2NH3(g)。反应过程中的部分数据如下表所示,下列说法正确的是
物质的量/ mol 时间/min | n(N2) | n(H2) | n(NH3) |
0 | 1.0 | 1.2 | 0 |
2 | 0.9 | ||
4 | 0.75 | ||
6 | 0.3 |
A. 0~2 min内,NH3的反应速率为0.1 mol·Lˉ1·minˉ1
B. 2 min时, H2的物质的量0.3 mol
C. 4 min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D. 4~6 min内,容器内气体分子的总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在周期表中的相对位置如图所示,已知X原子的最外层电子数为4。下列说法正确的是
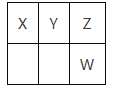
A. 元素Z的主要化合价:-2、+6
B. 原子半径:X>Y>Z
C. 最低价气态氢化物的稳定性:W>Z
D. 最高价氧化物对应的水化物的酸性:X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为探究加热条件下![]() 固体的分解反应,将一定量
固体的分解反应,将一定量![]() 固体在隔绝空气条件下充分加热,最终得到固体A。
固体在隔绝空气条件下充分加热,最终得到固体A。
(1)甲同学认为分解会产生![]() 气体,于是用________试纸检验反应后容器内气体,试纸颜色不变。
气体,于是用________试纸检验反应后容器内气体,试纸颜色不变。
(2)他们通过比较反应前后固体的水溶液在常温下的pH不同,初步证明了Na2SO3固体发生了分解:
①取a g Na2SO3固体配成100mL溶液,测溶液的pH1>7,用离子方程式表示其原因:__________。
②_________(填操作),测得溶液的pH2>pH1。
(3)该小组同学查阅资料并继续实验。资料显示:Na2SO3固体在隔绝空气加热时能分解得到两种盐;H2S是具有刺激性气味的气体,溶于水形成的氢硫酸是二元弱酸。
实验如下:
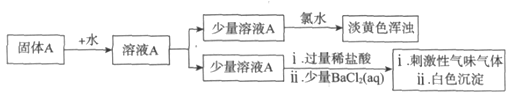
①加入氯水后的现象表明有硫单质生成,则说明固体A中含有_______离子。
②结合资料和实验,写出Na2SO3固体受热发生分解的化学方程式:____________。
(4)同学们根据(2)中pH2>pH1还得出结论:相同条件下HSO3-的电离能力强于HS-,理由是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com