
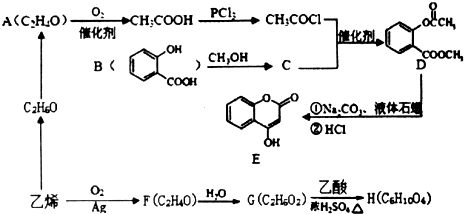
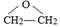 ����Ϊ����������Ҫ�����ᷢ��������Ӧ��1��2��Ӧ��F��G�ǿ����ӳɷ�Ӧ����GΪ�Ҷ������Ҷ��������ᷴӦ����H��C6H10O4����HΪ�������Ҷ���
����Ϊ����������Ҫ�����ᷢ��������Ӧ��1��2��Ӧ��F��G�ǿ����ӳɷ�Ӧ����GΪ�Ҷ������Ҷ��������ᷴӦ����H��C6H10O4����HΪ�������Ҷ���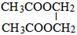 ���ݴ˽��
���ݴ˽��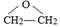 ����Ϊ����������Ҫ�����ᷢ��������Ӧ��1��2��Ӧ��F��G�ǿ����ӳɷ�Ӧ����GΪ�Ҷ������Ҷ��������ᷴӦ����H��C6H10O4����HΪ�������Ҷ���
����Ϊ����������Ҫ�����ᷢ��������Ӧ��1��2��Ӧ��F��G�ǿ����ӳɷ�Ӧ����GΪ�Ҷ������Ҷ��������ᷴӦ����H��C6H10O4����HΪ�������Ҷ���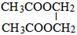 ��
��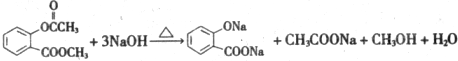 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��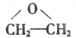 ��HΪ
��HΪ �ʴ�Ϊ��
�ʴ�Ϊ��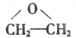 ��
�� ��
��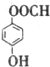 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��


 �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ʹpH��ֽ�ʺ�ɫ����Һ��Na+��NH4+��I-��NO3- |
| B��������������H2����Һ��K+��Mg2+��SO42-��HCO3- |
| C��c��Fe3+��=0.1mol?L-1����Һ��H+��Al3+��I-��SCN- |
| D��������pH=12����Һ��Na+��K+��SiO32-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ij��ɫ��Һ�н�����AgNO3��Һ���Լ���δ֪��Һ�е�Cl- |
| B����ij��Һ�еμ�ϡ����������ɫ���壬˵��ԭ��Һ����CO32- |
| C����ij��ɫ��Һ�н�����BaCl2��Һ���Լ���δ֪��Һ�е�SO42- |
| D����ʢ��Һ�����ƿ����ʱ����Ҫ�����Ƭ���ʯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2CO3 |
| B��K2CO3��Na2CO3 |
| C��NaOH��K2CO3 |
| D��K2CO3��NaOH��Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
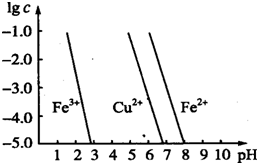 �����ȡ�ͭ���仯�������������������й㷺����;���Իش��������⣮
�����ȡ�ͭ���仯�������������������й㷺����;���Իش��������⣮| c(ClO2-) |
| c(HClO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2S��Һ |
| B��NaOH��Һ |
| C��AlCl3��Һ |
| D��CaCl2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 | B��2 |
| C������2 | D����1��2֮�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com