
��糧����ȼú���磬úȼ���е��Ȼ�ѧ����ʽ�У�C��s��+O2��g��═CO2��g����H1=﹣393.5kJ/molCO��g��+ O2��g��═CO2��g����H2=﹣283kJ/mol C��s��+
O2��g��═CO2��g����H2=﹣283kJ/mol C��s��+ O2��g��═CO��g����H3=�������й�˵���в���ȷ���ǣ���
O2��g��═CO��g����H3=�������й�˵���в���ȷ���ǣ���
A�� CO��ȼ����Ϊ283 kJ/mol
B�� ������̼�ֽ�Ϊһ����̼�������ķ�Ӧ�����ȷ�Ӧ
C�� ��H3=��H2﹣��H1=110.5 kJ/mol
D�� ��H3=��H1﹣��H2=﹣110.5 kJ/mol
���㣺 �ø�˹���ɽ����йط�Ӧ�ȵļ��㣮
ר�⣺ ��ѧ��Ӧ�е������仯��
������ A����CO��g��+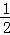 O2��g��═CO2��g����H2=﹣283kJ/mol�������֪CO��ȼ���ȣ�
O2��g��═CO2��g����H2=﹣283kJ/mol�������֪CO��ȼ���ȣ�
B��CO��g��+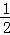 O2��g��═CO2��g����H2=﹣283kJ/mol��Ϊ���ȷ�Ӧ���淴ӦΪ���ȷ�Ӧ��
O2��g��═CO2��g����H2=﹣283kJ/mol��Ϊ���ȷ�Ӧ���淴ӦΪ���ȷ�Ӧ��
C��̼����ȫȼ��Ҳ�Ƿ��ȷ�Ӧ����H��0��
D����C��s��+O2��g��═CO2��g����H1=﹣393.5kJ/mol��CO��g��+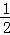 O2��g��═CO2��g����H2=﹣283kJ/mol�����ݸ�˹���ɢ�﹣�ڵ�C��s��+
O2��g��═CO2��g����H2=﹣283kJ/mol�����ݸ�˹���ɢ�﹣�ڵ�C��s��+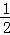 O2��g��═CO��g����H3��
O2��g��═CO��g����H3��
��� �⣺A��CO��g��+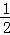 O2��g��═CO2��g����H2=﹣283kJ/mol��CO��ȼ����Ϊ283 kJ/mol����A��ȷ��
O2��g��═CO2��g����H2=﹣283kJ/mol��CO��ȼ����Ϊ283 kJ/mol����A��ȷ��
B��CO��g��+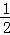 O2��g��═CO2��g����H2=﹣283kJ/mol��Ϊ���ȷ�Ӧ���淴ӦΪ���ȷ�Ӧ����B��ȷ��
O2��g��═CO2��g����H2=﹣283kJ/mol��Ϊ���ȷ�Ӧ���淴ӦΪ���ȷ�Ӧ����B��ȷ��
C��̼����ȫȼ��Ҳ�Ƿ��ȷ�Ӧ����H��0����C����
D����C��s��+O2��g��═CO2��g����H1=﹣393.5kJ/mol��CO��g��+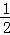 O2��g��═CO2��g����H2=﹣283kJ/mol�����ݸ�˹���ɢ�﹣�ڵ�C��s��+
O2��g��═CO2��g����H2=﹣283kJ/mol�����ݸ�˹���ɢ�﹣�ڵ�C��s��+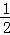 O2��g��═CO��g����H3�����ԡ�H3=��H1﹣��H2=﹣110.5 kJ/mol����D��ȷ��
O2��g��═CO��g����H3�����ԡ�H3=��H1﹣��H2=﹣110.5 kJ/mol����D��ȷ��
��ѡC��
������ ���⿼�黯ѧ��Ӧ�������������ڸ�˹���ɵ����ã�ע����ո�˹���ɵ�ԭ���Լ����㷽�����ѶȲ���


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪298Kʱ���ϳɰ���ӦN2��g�� +3H2��g��⇌2NH2��g����H=﹣92.0kj•mol﹣1�������¶��µ�lmol N2��3mol ����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������Ϊ���ٶ�����������û��������ʧ������
+3H2��g��⇌2NH2��g����H=﹣92.0kj•mol﹣1�������¶��µ�lmol N2��3mol ����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������Ϊ���ٶ�����������û��������ʧ������
A�� һ��С��92.0 kJ B�� һ������92.0 kJ
C�� һ������92.0 kJ D�� ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ���ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3X������+Y������═2Z������������������X��Y��Z����1mol����Ӧ��X��ƽ����Ӧ����Ϊ0.12mol•L﹣1•s﹣1����Ҫ����ZΪ1.8mol����Ӧ�����ʱ��Ϊ����
A�� 5s B�� 10s C�� 15s D�� 20s
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��H2O2��H2SO4�Ļ����Һ���ܳ��Ͼ�ӡˢ��·���ϵ�ͭ����֪��Cu��s��+2H+��aq��═Cu2+��aq��+H2��g����H1=+64.39kJ/mol2H2O2��l��═2H2O��l��+O2��g����H2=﹣196.46kJ/molH2��g��+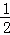 O2��g��═H2O��l����H3=﹣285.84kJ/mol����H2SO4��Һ�У�Cu��H2O2��Ӧ����Cu2+��aq����H2O��l���ķ�Ӧ��Ϊ���٣�
O2��g��═H2O��l����H3=﹣285.84kJ/mol����H2SO4��Һ�У�Cu��H2O2��Ӧ����Cu2+��aq����H2O��l���ķ�Ӧ��Ϊ���٣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������3���Ȼ�ѧ����ʽ��
2H2S��g��+3O2��g��=2SO2��g��+2H2O��l����H=﹣Q1 kJ/mol
2H2S��g��+O2��g��=2S��s��+2H2O��l����H=﹣Q2 kJ/mol
2H2S��g��+O2��g��=2S��s��+2H2O��g����H=﹣Q3 kJ/mol
�ж�Q1��Q2��Q3���߹�ϵ��ȷ���ǣ���
A�� Q1��Q2��Q3 B�� Q1��Q3��Q2 C�� Q3��Q2��Q1 D�� Q2��Q1��Q3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�Ȼ�ѧ����ʽC2H2��g��+ O2��g��═2CO2��g��+H2O��g����H=﹣1256kJ/mol������˵����ȷ���ǣ���
O2��g��═2CO2��g��+H2O��g����H=﹣1256kJ/mol������˵����ȷ���ǣ���
A�� ��Ȳ��C2H2����ȼ����Ϊ1256 kJ/mol
B�� ��ת��10 mol���ӣ�������2.5 mol O2
C�� ������2 molҺ̬ˮ�����H=﹣2512 kJ/mol
D�� ���γ�4 mol̼�����õ��Ӷԣ���ų�������Ϊ2512 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ������̫���ֽܷ�ˮ���ɵ������ڴ�����������CO2��Ӧ���ɼ״���CH3OH������������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�أ���֪H2��g����CO��g����CH3OH��l����ȼ���ȡ�H�ֱ�Ϊ﹣285.8kJ/mol��﹣283.0kJ/mol��﹣726.5kJ/mol����ش��������⣺
��1����̫���ֽܷ�5molˮ���ĵ������� kJ��
��2���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽΪ ��
��3����֪25�桢101kPa�£�H2O��l��═H2O��g����H=+44kJ•mol﹣1����1g�״���CH3OH��ȼ�� ����CO2����̬ˮʱ�ų�������Ϊ ��
����CO2����̬ˮʱ�ų�������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ�Ͽ����úϳ�����CO��H2�Ļ�����壩�����״�����֪��CO��g��+2H2��g��⇌CH3OH��g����H=﹣92.9kJ/molһ�������£��÷�Ӧ��һ����̶����ܱ������дﵽƽ�⣮����˵����ȷ���ǣ���
A�� �÷�Ӧ�ġ�S��0
B�� �÷�Ӧ���κ��¶��¾����Է�����
C�� �������г�������He��ƽ��������Ӧ�����ƶ�
D�� �����¶�ƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1 Lˮ������Mg(HCO3)2��CaCl2��Ũ�ȷֱ���b mol��L��1��2b mol��L��1������һ���Լ�(����)��Ca2����Mg2����ȥ�������Լ����ѡ�� (����)��
A��Ca(OH)2 B��NaOH
C��NaHCO3 D��Na2CO3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com