
除去下列物质中的杂质(括号内是杂质),能采用先与过量NaOH溶液充分反应再过滤的方法的是( )
A.Fe3O4(Al2O3) B.KCl(NaCl)
C.SiO2(CaCO3) D.FeCl2溶液(FeCl3)
科目:高中化学 来源: 题型:
下列根据实验现象所得出的结论不正确的是( )
A.无色溶液使紫色石蕊试液变蓝;结论:溶液一定呈碱性
B.无色溶液焰色反应呈紫色(透过蓝色钴玻璃观察),结论:溶液中一定含有K+
C.在无色溶液中加入Na2CO3溶液产生白色沉淀;结论:溶液中一定含有Ca2+
D.在无色盐溶液中加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝;结论:溶液一定含有NH
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废气中的氮氧化物(如NO、NO2等,用通式NOx表示)是主要的大气污染物之一.为了保护环境,工业上常通入氨气与之发生如下反应:NOx+NH3—→N2+H2O来消除污染.有关此反应,下列说法中错误的是
A.N2既是氧化产物又是还原产物
B.当x=1时,每生成2.5 mol N2,被氧化的气体有3 mol
C.当x=2时,有1 mol气体被还原,转移电子4 mol
D.反应通式配平表示为:6NOx+4xNH3===(3+2x)N2+6xH2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列依据热化学方程式得出的结论正确的是( )
A.已知2SO2(g)+O2(g)2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C.已知H+(aq)+OH-(aq)===H2O(l)
ΔH=-57.3 kJ·mol-1,则任何酸碱中和反应的热效应均为57.3 kJ
D.已知2C(s)+2O2(g)===2CO2(g) ΔH1,2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
1918年,Lewis提出反应速率的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞。
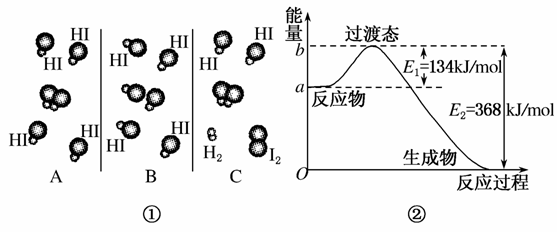
(1)图①是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(选填“A”、“B”或“C”)。
(2)20世纪30年代Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。图②是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________________________________________________________
______________________________________________________________。
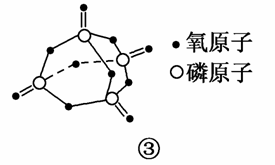
(3)过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化。请在图②中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图。
(4)进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,下表是部分化学键的键能数据:
| 化学键 | P—P | P—O | O===O | P===O |
| 键能/kJ·mol-1 | 197 | 360 | 499 | x |
已知白磷的燃烧热为2 378.0 kJ/mol,白磷完全燃烧的产物结构如图③所示,则上表中x=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
能在水溶液中大量共存的一组离子是( )
A.H+、I-、NO 、SiO
、SiO
B.Ag+、Fe3+、Cl-、SO
C.K+、SO 、Cu2+、NO
、Cu2+、NO
D.NH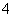 、OH-、Cl-、HCO
、OH-、Cl-、HCO
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外研究小组用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程如图所示:

(1)杂铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于________上(填写下列所给仪器的编号,下同),取用坩埚应使用________,灼烧后的坩埚应放在________上,不能直接放在桌面上。
实验所用仪器:
a.蒸发皿 b.石棉网 c.泥三角 d.表面皿
e.坩埚钳 f.试管夹
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是________(填选项字母)。
a.灼烧过程中部分氧化铜被还原
b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解生成铜
d.该条件下铜无法被氧气氧化
(3)通过途径Ⅱ实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤有:酸溶、加热通氧气、过滤、________、冷却结晶、________、自然干燥。
(4)由粗制氧化铜通过两种途径制取胆矾,与途径Ⅰ相比,途径Ⅱ有明显的两个优点是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)25 ℃、101 kPa时,1 g甲醇完全燃烧生成CO2和液态水,放出22.68 kJ热量,则该反应的热化学方程式为________________________________________。
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在O2中燃烧,生成固态B2O3和液态水,放出649.5 kJ热量,则该反应的热化学方程式为_____________
___________________________________________________________。
(3)肼(N2H4)是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量,则肼燃烧的热化学方程式为______
_______________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.碳酸氢镁溶液加入过量氢氧化钠:
B.碳酸钡溶于醋酸溶液: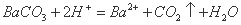
C.次氯酸钙溶液中通入少量二氧化碳: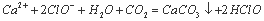
D.氧化铁加入氢碘酸中: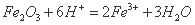
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com