
【题目】广东省有着丰富的海洋资源。海水提取食盐和Br2以后的盐卤可以用来制备纯净的MgCl2或MgO。盐卤中含有Mg2+、Cl-,还含有少量Na+、Fe2+、Fe3+和CO(NH2)2等.制备流程如图所示:
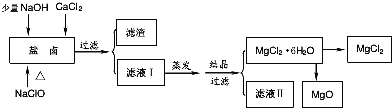
(1)滤渣的成分是____________(填化学式);滤液Ⅱ中所含的主要杂质离子是________(写离子符号)。
(2)用NaClO除去尿素CO(NH2)2时,生成物除盐外,都是能参与大气循环的物质,则该反应的化学方程式为_____________________;
(3)用MgCl26H2O制备无水MgCl2过程中,所需要的化学试剂是___________________;
(4)海水制溴过程中吸收潮湿空气中的Br2是利用SO2气体,SO2吸收Br2的离子方程式是_______________;SO2气体可来源于硫酸工业的尾气,同时,SO2尾气也可用氨水吸收,作为制备化肥的原料,SO2气体用氨水吸收得到的产物可能是___________________________。
【答案】Fe(OH)3 Na+ 3NaClO+CO(NH2)2═3NaCl+CO2↑+N2↑+2H2O或NaOH+3NaClO+CO(NH2)2═3NaCl+NaHCO3+N2↑+2H2O HCl气体 SO2+Br2+2H2O═4H++SO42-+2Br- (NH4)2SO3或NH4HSO3
【解析】
向盐卤溶液中加入NaClO,NaClO具有强氧化性,能将Fe2+氧化为Fe3+,向盐卤中加入少量NaOH,NaOH和Fe3+反应生成Fe(OH)3,CO(NH2)2和NaClO发生氧化还原反应,生成物除盐外,都是能参与大气循环的物质,所以生成物是NaCl、CO2、N2、H2O,过量二氧化碳能和NaOH反应生成碳酸氢钠,将溶液过滤得到的滤渣是Fe(OH)3,滤液I中含有Mg2+、Cl-、Na+,将滤液I蒸发、结晶、过滤得到MgCl26H2O,则滤液中含有的杂质离子是Na+,直接将MgCl26H2O加强热能得到MgO,发生反应MgCl26H2O![]() MgO+2HCl↑+5H2O↑,氯化镁易水解,所以不能用加热MgCl26H2O方法制取氯化镁,要在HCl氛围中制取氯化镁;
MgO+2HCl↑+5H2O↑,氯化镁易水解,所以不能用加热MgCl26H2O方法制取氯化镁,要在HCl氛围中制取氯化镁;
(1)通过以上分析知,滤渣是Fe(OH)3,滤液II中杂质离子是Na+;
(2)通过以上分析知,该反应为3NaClO + CO(NH2)2 ═ 3NaCl + CO2↑ + N2↑ + 2H2O或NaOH + 3NaClO + CO(NH2)2 ═ 3NaCl + NaHCO3 + N2↑ + 2H2O;
(3)氯化镁易水解,为防止氯化镁水解,在制取氯化镁时,要将MgCl26H2O放在氯化氢气体中;
(4)溴具有强氧化性,二氧化硫具有还原性,二者在水溶液里能发生氧化还原反应生成硫酸和氢溴酸,离子反应方程式为SO2+Br2+2H2O═4H++SO42-+2Br-,当二氧化硫少量时,二者反应生成(NH4)2SO3,当二氧化硫过量时,二者反应生成NH4HSO3。
【点晴】
准确的流程分析是解题关键,向盐卤溶液中加入NaClO,NaClO具有强氧化性,能将Fe2+氧化为Fe3+,向盐卤中加入少量NaOH,NaOH和Fe3+反应生成Fe(OH)3,CO(NH2)2和NaClO发生氧化还原反应,生成物除盐外,都是能参与大气循环的物质,所以生成物是NaCl、CO2、N2、H2O,过量二氧化碳能和NaOH反应生成碳酸氢钠,将溶液过滤得到的滤渣是Fe(OH)3,滤液I中含有Mg2+、Cl-、Na+,将滤液I蒸发、结晶、过滤得到MgCl26H2O,则滤液中含有的杂质离子是Na+,直接将MgCl26H2O加强热能得到MgO,发生反应MgCl26H2O![]() MgO+2HCl↑+5H2O↑,氯化镁易水解,所以不能用加热MgCl26H2O方法制取氯化镁,要在HCl氛围中制取氯化镁;据此可解答。
MgO+2HCl↑+5H2O↑,氯化镁易水解,所以不能用加热MgCl26H2O方法制取氯化镁,要在HCl氛围中制取氯化镁;据此可解答。


科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:X2(g)+Y2(g)![]() 2Z(g),若X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡状态时,下列说法正确的是
2Z(g),若X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡状态时,下列说法正确的是
A、Z的浓度可能为0.3mol/L
B、平衡时X2、Y2的转化率相等
C.平衡时,Y2和Z的生成速率之比为2:1
D、若平衡后再改变外界条件,升高温度,则反应的平衡常数将变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组探究在加热条件下FeSO4分解的气体产物及相关性质。已知:SO2的沸点为-10 ℃、SO3的沸点为44.8 ℃。
用如图所示装置设计实验,验证分解FeSO4生成的气态产物。
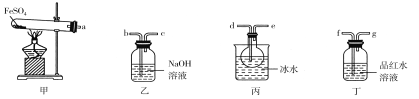
(1)实验前必须进行的操作是________。
(2)按气流方向连接各仪器,用字母表示接口的连接顺序:a→________。
(3)若观察到装置甲中固体变为红棕色,装置丙中有无色液体产生,装置丁中溶液变成无色,则FeSO4分解的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是![]()
A.在蒸馏水中滴加浓![]() ,
,![]() 不变
不变
B.向![]() 溶液中滴加
溶液中滴加![]() 溶液,有沉淀和气体生成
溶液,有沉淀和气体生成
C.中和等体积等物质的量浓度的盐酸和醋酸,所消耗的氢氧化钠的物质的量相同
D.![]() 相等的
相等的![]() 溶液和
溶液和![]() 溶液,两溶液中水的电离程度相同
溶液,两溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1)设计实验方案来研究影响化学反应速率的因素。甲同学的实验报告如下表:
实验步骤 | 现象 | 结论 |
①分别取等体积的2 mol·L-1的硫酸于试管中 | 反应速率Mg>Fe,Cu不反应 | 金属的性质越活泼,反应速率越快 |
②____________ | 反应物浓度越大,反应速率越快 |
(1)甲同学表中实验步骤②为_________________________________________。
(2)甲同学的实验目的是_____________;要得出正确的实验结论,还需控制的实验条件是____________。乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。

(3)乙同学在实验中应该测定的数据是___________________________________________________。
(4)乙同学完成该实验应选用的实验药品是________,该实验中不选用某浓度的硫酸,理由是___________。
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是______________的影响。
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是________(填字母)。
A.硫酸钾 B.硫酸锰 C.二氯化锰 D.水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以环戊烷为原料制备环戊二烯的合成路线如图,则下列说法正确的是( )
![]()
A. A的结构简式是![]()
B. ①②的反应类型分别是取代、消去
C. 反应②③的条件分别是浓硫酸加热、光照
D. 加入酸性KMnO4溶液,若溶液褪色则可证明![]() 已完全转化为
已完全转化为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生产、生活密切相关.下列说法不正确的是![]()
A.医学上,血液透析是利用了胶体的渗析原理
B.碳酸氢钠可用于制备纯碱,作治疗胃酸过多的药物及食品发酵剂
C.高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强
D.铜的金属性比铝弱,可以用铜罐贮运浓硝酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中各微粒的浓度关系正确的是
A.等pH的醋酸溶液、盐酸溶液、硫酸溶液中:![]()
B.将10mL![]()
![]() 的
的![]() 溶液逐滴滴加到10mL
溶液逐滴滴加到10mL![]()
![]() 的盐酸中:
的盐酸中:![]()
C.向![]() 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至![]() :
:![]()
D.![]()
![]() 的某一元弱酸HA溶液和
的某一元弱酸HA溶液和![]()
![]() 溶液等体积混合后的溶液:
溶液等体积混合后的溶液:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的硫酸钡放入水中,有关的叙述正确的是( )
A.硫酸钡不溶于水,硫酸钡固体质量不会改变
B.最终会得到BaSO4的极稀的饱和溶液
C.因为![]() 很容易发生,所以不存在BaSO4(s)
很容易发生,所以不存在BaSO4(s)![]() Ba2+(aq)+SO42-(aq)的过程
Ba2+(aq)+SO42-(aq)的过程
D.因为BaSO4难溶于水,所以改变外界条件也不会改变BaSO4的溶解性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com