
【题目】 是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如下图所示:
是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如下图所示:

已知:

(1)A的结构简式为_____________,B的化学名称为_____________。
(2)由C生成D的反应类型为_____________。
(3)反应①的反应条件_____________。
(4)反应③的化学方程式为_____________。
(5)与D互为同分异构体且含有碳碳双键和-COO-的苯的二元取代物有_____种,其中核磁共振谱为5组峰,且峰面积比为2:1:2:2:1的结构简式为______________(任写一种)。
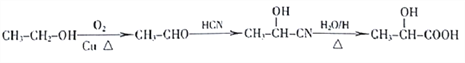
(6)写出以C2H5OH为原料合成乳酸( )的路线______________ (其他试剂任选,合成路线常用的表示方式为
)的路线______________ (其他试剂任选,合成路线常用的表示方式为![]() )
)
【答案】 HCHO 苯乙醛 消去反应 NaOH醇溶液,加热 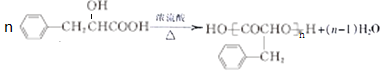 6
6 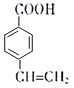 或
或
【解析】根据流程图知,①为消去反应、②为加成反应、③发生信息i的氧化反应,则A为HCHO、B为![]() ,B发生信息ii的反应,C结构简式为
,B发生信息ii的反应,C结构简式为![]() ,C发生缩聚反应生成E,E结构简式为
,C发生缩聚反应生成E,E结构简式为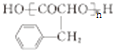 ,C发生消去反应生成D,D结构简式为
,C发生消去反应生成D,D结构简式为![]() ,D和苯酚发生酯化反应生成
,D和苯酚发生酯化反应生成![]() 。
。
(1)根据上述分析,A为HCHO,B为![]() ,名称为苯乙醛,故答案为:HCHO;苯乙醛;
,名称为苯乙醛,故答案为:HCHO;苯乙醛;
(2)C在浓硫酸体积下发生消去反应生成D,故答案为:消去反应;
(3)根据流程图,反应①是卤代烃发生消去反应生成烯烃,反应条件为NaOH醇溶液,加热,故答案为:NaOH醇溶液,加热;
(4)反应③是C发生的缩聚反应,反应的化学方程式为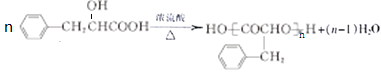 ,故答案为:
,故答案为: ;
;
(5) D为![]() ,与D互为同分异构体且含有碳碳双键和-COO-的苯的二元取代物有
,与D互为同分异构体且含有碳碳双键和-COO-的苯的二元取代物有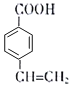 (包括邻位、间位、对位3种)和
(包括邻位、间位、对位3种)和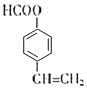 (包括邻位、间位、对位3种),共6种;其中核磁共振谱为5组峰,且峰面积比为2:1:2:2:1的结构简式为
(包括邻位、间位、对位3种),共6种;其中核磁共振谱为5组峰,且峰面积比为2:1:2:2:1的结构简式为 和
和 ,故答案为:6;
,故答案为:6; 和
和 ;
;
(6)CH3CH2OH被催化氧化生成CH3CHO,CH3CHO和HCN发生加成反应生成CH3CH(OH)CN,该物质发生水解反应生成CH3CH(OH)COOH,其合成路线为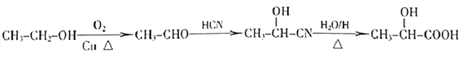 ,故答案为:
,故答案为: 。
。


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】分子式为C2H4O2的所有同分异构体在下列—种表征仪器中显示的信号(或数据)完全相同,则该仪器是( )
A. 质谱仪 B. 红外光谱仪 C. 元素分析仪 D. 核磁共振仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是在实验室中模拟“氨碱法”制取![]() 的部分装置。
的部分装置。

完成下列填空:
(1)仔细观察两只通气导管在瓶内所处的位置,由此推断:气体a为___________,气体b为_____________;两者的通入次序为_____________。为防止尾气污染,c中可放入蘸__________溶液的脱脂棉。
(2)气体a与b均可用如图装置进行制备。

当锥形瓶中固定为生石灰时,分液漏斗中应盛放____________。
用该装置制备另一种气体的方法是(用离子方程式表示):______________________。
(3)反应过程中可以看到装置饱和食盐水中有晶体逐渐析出,写出相关反应的化学方程式:__________________。
(4) 反应过程中采用水浴加热,其优势是_______________。
水浴温度维持在42℃左右,温度过低,反应速率太慢,不利于晶体析出;温度过高,________________,也不利于晶体析出。
(5)反应结束后,将热水浴换成冰水浴,冷却15min左右再进行过滤,目的是:
___________________。
(6)得到的![]() 晶体中会含有少量
晶体中会含有少量![]() 杂质,可采用如下方法进行纯度测定:
杂质,可采用如下方法进行纯度测定:

该试样中![]() 的质量分数为_____________(精确到0.01)。
的质量分数为_____________(精确到0.01)。
若称量操作无误,但最终测定结果的相对误差为1.5%,写出可能导致该结果的一种情况。________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物①~⑩的名称、分子式或结构简式为:
①C2H2 ②新戊烷 ③甲苯 ④![]()
⑤![]() ⑥CH3CH(C2H5)CH2CH(C2H5)CH3 ⑦C5H10
⑥CH3CH(C2H5)CH2CH(C2H5)CH3 ⑦C5H10
⑧ClCH=CHCl ⑨C5H4 ⑩![]()
(1)其中互为同系物的是________(填序号),一定存在顺反异构的是__________(填序号)。
(2)⑥可由单烯烃与H2加成得到,该单烯烃可能有_______种结构。
(3)氯气与③在光照条件下生成一氯代物的化学反应方程式:_____________。
(4)③的同系物A,分子中共含66个电子,A苯环上一溴代物只有一种,请写出A的结构简式_________。
(5)⑨理论上同分异构体的数目可能有30多种。
如:A.CH2=C=C=C=CH2 B.CH≡C-CH=C=CH2
C. ![]() D.
D. ![]() E.
E. ![]()
请写出所有碳原子均共线的一种链状分子的结构简式:__________(写一种即可)。
(6)⑩分子中最多有______个原子共面。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸镁可用于牙膏、医药化妆品等工业,化学式为4MgCO3·Mg(OH)2·5H2O,某碱式碳酸镁中含有SiO2杂质,为测定其纯度。某兴趣小组设计了如下几个方案:
方案1
取一定质量的样品,与硫酸充分反应,通过测定CO2的质量计算纯度

(1)乙中发生反应的方程式为______________________________ 。
(2)仪器接口的连接顺序为(装置可以重复使用) a___________,丁的作用是__________________。
(3)关闭止水夹K,向样品中加入足量的稀硫酸,当样品充分反应完后,为了测定准确还应进行的操作是______________________________。
方案Ⅱ
①称取碱式碳酸镁样品mg;②将样品充分高温燃烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g(用托盘天平称量)。
(4)下列仪器中,该方案不会用到的是____________。

(5)判断样品完全分解的方法是_________________________。
(6)有同学认为方案Ⅱ高温燃烧的过程中会发生![]()
会导致测定结果有误,你任为这位同学的观点正确吗?_________,(填“正确”或“错误”)
请说明自己的理由:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某元素+2价离子的电子排布式为1s22s22p63s23p6,则该元素在周期表中属于( )
A. 第ⅤB族B. 第ⅡB族C. 第Ⅷ族D. 第ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中能大量共存,且溶液为无色透明的离子组是
A.Na+、Al3+、SO42—、NO3- B.Ba2+、Na+、SO42—、NO3-
C.K+、Mg2+、MnO4—、SO42—、 D.K+、Na+、NO3- 、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质C(s)的燃烧热为Y kJ/mol,则1 mol C(s)与O2(g)反应生成CO(g)的反应热ΔH为( )
A.-Y kJ/mol B.-(10X-Y)kJ/mol
C.-(5X-0.5Y) kJ/mol D.+(10X-Y)kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com