
| A. | 乙炔的燃烧热为1256 kJ/mol | |
| B. | 若转移10 mol电子,则消耗2.5 mol O2 | |
| C. | 若生成2 mol 液态水,则△H=-1256 kJ/mol | |
| D. | 若形成4 mol碳氧共用电子对,则放出的热量为1256 kJ |
分析 A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量;
B、依据氧化还原反应电子守恒计算分析计算;
C、气态水变为液态水放热;
D、形成4mol碳氧共用电子对是形成1mol二氧化碳.
解答 解:A、热化学方程式中水是气体不是稳定的氧化物,所以燃烧热应大于1256kJ/mol,故A错误;
B、依据反应化学方程式可知消耗2.5mol氧气,电子转移为10mol,故B正确;
C、气态水变为液态水放热,若生成2mol液态水,则△H<-1256kJ/mol,故C错误;
D、若形成4mol碳氧共用电子对,即生成1mol二氧化碳,则放出的热量为$\frac{1256}{4}$kJ=314kJ,故D错误;
故选B.
点评 本题考查了燃烧热的概念分析判断,氧化还原反应的电子转移计算应用,盖斯定律的应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 乙醇和乙酸 | B. | 金刚石和石墨 | ||
| C. | ${\;}_{8}^{16}$O和${\;}_{8}^{17}$O | D. | CH3CH2CH2CH3和 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,氧化剂是氯酸钾,还原产物是Cl2.
,氧化剂是氯酸钾,还原产物是Cl2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 儿童牙膏 | 防臭牙膏 | 透明牙膏 | |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 氧化硅 |
| 物质类别 | 碱 | 盐 | 氧化物 |
 ,请写出氟化钠在水溶液中的电离方程式NaF=Na++F-.
,请写出氟化钠在水溶液中的电离方程式NaF=Na++F-.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2HI(g)?H2(g)+I2(g)△H<0 | B. | N2(g)+3H2(g)?2NH3(g)△H<0 | ||
| C. | C(s)+H2O(g)?CO(g)+H2(g)△H>0 | D. | CaCO3(s)?CO2(g)+CaCO3(s)△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
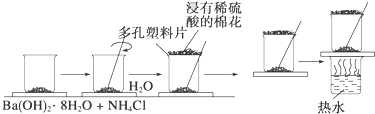
| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 ①产生 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 ②反应 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 ③生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
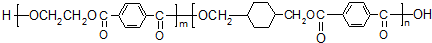
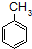 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$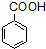
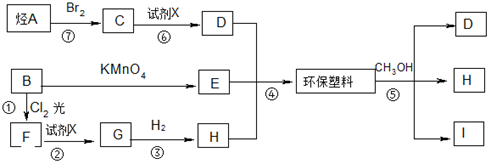
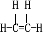 ;
;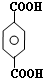 ;B的名称:对二甲苯,试剂X为NaOH水溶液.
;B的名称:对二甲苯,试剂X为NaOH水溶液.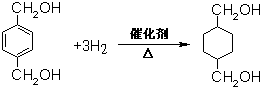 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学平衡常数是指在一定温度下生成物浓度幂之积与反应物浓度幂之积的比值 | |
| B. | 勒夏特列原理指的是,如果改变影响平衡的条件之一(如温度、压强、参与反应物质的浓度,),平衡将向着能够减弱这种改变的方向移动 | |
| C. | 盐溶液不一定呈中性,不显中性的盐都会促进水的电离 | |
| D. | 把被保护的钢铁设备作为电解池的阴极,该方法称为牺牲阳极的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 反应物 | CO2 | Fe2O3 | C2H5OH | FeCl3 |
| 生成物 | MgO | Al2O3 | C2H5ONa | CuCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com