
根据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如图所示,其中盐桥为琼脂-饱和KNO3盐桥。

请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________;
(2)银电极为电池的____极,写出两电极的电极反应式:
银电极:____________;X电极:____________。
(3)外电路中的电子是从______电极流向______电极。
(4)盐桥中向CuSO4溶液中迁移的离子是________(填序号)。
A.K+ B.NO
C.Ag+ D.SO
科目:高中化学 来源: 题型:
Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第________周期第________族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为________________________。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si____S | O2-____Na+ | NaCl____Si | H2SO4____HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是________________________________________________________________________
________________________________________________________________________。
(4)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的同学们按照下面的实验方法制备氢氧化铁胶体:首先取少量蒸馏水于洁净的烧杯中,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的FeCl3溶液继续煮沸,至液体呈透明的红褐色。
FeCl3+3H2O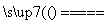 Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(1)判断胶体制备是否成功,可利用胶体的____________________。
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到________________,其原因是______________________________________________________________。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会________________,原因是__________________________________________
____________________________________________________。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会_______ _________,原因是_________________________________________
_________,原因是_________________________________________
_______________________________________________________。
(3)丁同学按要求制备了Fe(OH)3胶体,但是他又向Fe(OH)3胶体中逐滴加入了稀H2SO4溶液,结果出现了一系列变化。
①先出现红褐色沉淀,原因是___________________________________
________________________________________________________。
②随后沉淀溶解,此反应的离子方程式为_________________________
__________________________ ________________________________。
________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在盛有KI溶液的试管中,滴入适量氯水充分反应后,再加四氯化碳振荡,静置后观察到的现象是( )
A.上层紫红色,下层接近无色
B.均匀、透明,紫红色
C.均匀、透明,无色
D.上层接近无色,下层紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
全球核安全峰会在华盛顿举行,发展核电、制裁核武器发展是会议主题。各式各样电池的发展是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
( )
A.手机上用的锂离子电池属于一次电池
B.锌锰干电池中,锌电极是负极
C.氢氧燃料电池工作时氢气在负极被还原
D.太阳能电池的主要材料为二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下图所示的四个原电池装置,结论正确的是( )
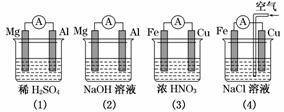
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极
B.(2)中Mg作正极,电极反应式为:6H2O+6e-===6OH-+3H2↑
C.(3)中Fe作负极,电极反应式为:Fe-2e-===Fe2+
D.(4)中Cu作正极,电极反应式为:2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐。现将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合液中,铜片完全溶解(不考虑盐的水解及溶液体积的变化)
(1)写出铜溶解于上 述混合液的离子方程式_____________________________。
述混合液的离子方程式_____________________________。
(2)若铜完全溶解时,溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶解铜的质量是________ g,溶液中的c(SO )=________ mol/L。
)=________ mol/L。
(3)若欲在如图所示的装置中发生(1)中的反应,请判断图中的正、负极,并选出适当的物质作电极,写出电极反应式,填在相应的表格中。

| 正、负极判断 | 电极材料 | 电极反应式 | |
| X极 | |||
| Y极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在第3周期中,置换酸中氢的能力最强的元素的元素符号为 ,化学性质最稳定的元素符号是 ,最高价氧化物的水化物的酸性最强的化合物的化学式是 ,最高价氧化物的水化物的碱性最强的化合物的化学式是 ,显两性的氢氧化物的化学式是 ,该两性氢氧化物与盐酸、氢氧钠溶液分别反应的离子方程式为 、 ,原子半径最大的金属元素的名称是 ,离子半径最小的离子结构示意图是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用镁铝合金制作的窗框、卷帘门、防护栏等物品轻巧、美观、耐用。与上述这些特点无关的镁铝合金的性质是 ( )
A.不易生锈 B.导电性好 C.密度小 D.强度高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com