
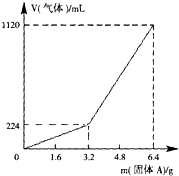
 ��һ������Ͼ��ȵ�����������ڸ��������������¹��ȣ���ַ�Ӧ����ȴ�����£��õ�����A��������Ϊm�Ĺ���A���뵽300mL 2mol?L-1������ʹ֮��ȫ�ܽ⣮��������¼������A���������ռ�������������ѻ���ɱ�״�����Ĺ�ϵ��ͼ15��ʾ������������������Һ����ǰ�����������ݳ�����
��һ������Ͼ��ȵ�����������ڸ��������������¹��ȣ���ַ�Ӧ����ȴ�����£��õ�����A��������Ϊm�Ĺ���A���뵽300mL 2mol?L-1������ʹ֮��ȫ�ܽ⣮��������¼������A���������ռ�������������ѻ���ɱ�״�����Ĺ�ϵ��ͼ15��ʾ������������������Һ����ǰ�����������ݳ�����| m |
| M |
| n |
| V |
| mg |
| 3.2g |


 53���ò�ϵ�д�
53���ò�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

 �������Լ�x��
�������Լ�x���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��c��C2O42-��+c��HC2O4-��+c��OH-��=c��K+��+c��H+�� |
| B��c��C2O42-��+c��HC2O4-��+c��H2C2O4��=0.2mol/L |
| C��c��C2O42-����c��HC2O4-����c��H2C2O4�� |
| D��c��H+����c��HC2O4-����c��C2O42-����c��K+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �������������ѧ��Fulvio Cacace�����ܰ����ӽṹ�������ֺϳ��˺Ͱ����Ӽ������Ƶ�N4���ӣ���֪����1mol N-N��������167kJ������������1mol N��N���ų�942kJ���������ж�����˵����ȷ���ǣ�������
�������������ѧ��Fulvio Cacace�����ܰ����ӽṹ�������ֺϳ��˺Ͱ����Ӽ������Ƶ�N4���ӣ���֪����1mol N-N��������167kJ������������1mol N��N���ų�942kJ���������ж�����˵����ȷ���ǣ�������| A��N4ת��ΪN2�Ĺ�����һ�����ȹ��� |
| B��N4�ķе��P4�����ף��ĸ� |
| C��N4��N2��Ϊͬ���칹�� |
| D��N4��������ԭ�Ӿ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1molOH-�����ת�Ƶ�����Ϊ0.1NA |
| B������ʽΪC2H6O���л���4.6g��������C-H������һ��Ϊ0.6NA |
| C����֪2SO2��g��+O2��g���T2SO3��g������H=-196.6kJ/mol����2NA��SO2��g����NA��O2��g�������ܱ������У���һ�������³�ַ�Ӧ�����ʱ�Ϊ-196.6kJ/mol |
| D���ڷ�Ӧ5NH4NO3�T2HNO3+4N2+9H2O�У�����15NA������ת�ƣ������������뻹ԭ��������ʵ���֮��Ϊ3��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A����������NaCl��Һ��pH�½� |
| B����Һ��Na+�����缫�����ƶ� |
| C��ͨ��һ��ʱ��ɿ���ʯī�缫������Һ��� |
| D��ͨ��һ��ʱ��ɿ����Թ�����Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe2+ |
| B��Ba2+ |
| C��C1- |
| D��Mg2+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com