
【有机物化学基础】
A-G均为有机化合物,其中A为二卤代烃,相对分子质量为216,碳的质量分数为22.2%。相关转化关系如下:
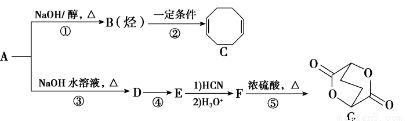
已知: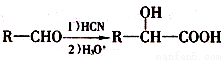
请回答:
(1)C的核磁共振氢谱有_______个吸收峰。
(2)①、④的反应类型分别为________、______。
(3)下列关于F的说法正确的是_______ (填选项字母)。
a.1 mol F与足量金属钠反应最多生成2 mol H2
b.1 mol F完全燃烧消耗8.5 mol O2
c.能与新制Cu(OH)2反应生成砖红色沉淀
d.能与NaHCO3反应生成CO2
(4)写出下列反应的化学方程式
反应③___________________________________;
反应⑤___________________________________;
(5)符合下列条件的同分异构体有_____种,任写其中一种的结构简式_____。
i.与E互为同系物 ii.相对分子质量比E大28
(1)2
(2)消去反应 氧化反应
(3)a d
(4)BrCH2CH2CH2CH2Br + 2NaOH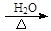 HOCH2CH2CH2CH2OH +2NaBr
HOCH2CH2CH2CH2OH +2NaBr
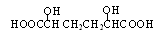
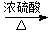
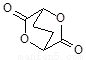 +2H2O
+2H2O
(5) 9
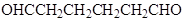
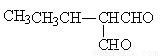
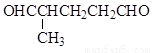
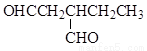
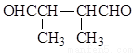
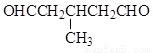
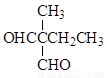
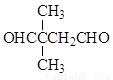
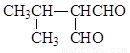
任写一种即可
【解析】A的相对分子质量为216,含碳质量分数为22.2%,则A中的碳原子数为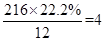 。根据A→B→C的变化,及C的结构简式可知,B为1,4-丁二烯,A的分子式可写为C4H8X2,则X的相对原子质量为80,X为Br;根据G的结构,可推知F的结构为
。根据A→B→C的变化,及C的结构简式可知,B为1,4-丁二烯,A的分子式可写为C4H8X2,则X的相对原子质量为80,X为Br;根据G的结构,可推知F的结构为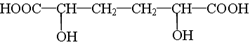 ,根据已知信息,可知E为HOC—CH2—CH2—CHO,则逆推可知D为OHCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br。
,根据已知信息,可知E为HOC—CH2—CH2—CHO,则逆推可知D为OHCH2CH2CH2CH2OH,则A为BrCH2CH2CH2CH2Br。
(1)C是对称结构,分子中只有2种H,因此核磁共振氢谱只有2组峰。
(2)A→B是卤代烃生成烯烃的消去反应,D→E是醇被氧化生成醛。
(3)F的结构简式为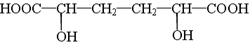 ,分子中的羟基、羧基均可与Na反应,因此1molF与Na反应可生成2mol H2,a正确;F的分子式为C6H10O6,1molF燃烧的耗氧量为
,分子中的羟基、羧基均可与Na反应,因此1molF与Na反应可生成2mol H2,a正确;F的分子式为C6H10O6,1molF燃烧的耗氧量为 mol,b错;F中不含醛基,不能与新制Cu(OH)2反应,c错;F中的羧基可与NaHCO3反应生成CO2,d正确。
mol,b错;F中不含醛基,不能与新制Cu(OH)2反应,c错;F中的羧基可与NaHCO3反应生成CO2,d正确。
(4)反应③为卤代烃水解产生醇,反应⑤为醇、羧酸的酯化。
(5)与E互为同系物,则含有的官能团种类、数目相同,相对分子质量比E大28,则分子式比E多C2H4,据此可写出该有机物的同分异构体。


科目:高中化学 来源:2014高考名师推荐化学--预测15 题型:选择题
已知(HF)2(g)  2HF(g) ΔH>0,且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
2HF(g) ΔH>0,且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强的变化曲线如图所示。下列说法正确的是
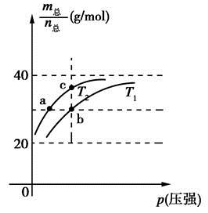
A.温度:T1<T2
B.平衡常数:K(a)=K(b)<K(c)
C.反应速率:vb>va
D.当 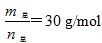 时,n(HF):n[(HF)2]=2:1
时,n(HF):n[(HF)2]=2:1
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测13 题型:选择题
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验:

A.步骤Ⅰ中减少的3 g固体一定是混合物
B.步骤Ⅱ中质量减少的物质一定是Cu
C.根据步骤Ⅰ、Ⅱ可以判断混合物X的成分为Al2O3、Fe2O3、Cu、SiO2
D.根据上述步骤Ⅱ可以得出m(Fe2O3)∶m(Cu)=1∶1
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测12 题型:选择题
下列说法不正确的是
A.已知H2(g)+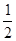 O2(g)===H2O(g) ΔH1=a kJ·mol-1;
O2(g)===H2O(g) ΔH1=a kJ·mol-1;
2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1,则a>b
B.CO的燃烧热为283.0 kJ·mol-1,则
2CO2(g)===2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1
C.若N2(g)+3H2(g)  2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ
D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和KOH反应的中和热ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:推断题
A、B、C、D四种物质溶于水均完全电离,电离出的离子如下表。
阳离子 | Na+、Al3+、Ba2+、H+、NH4+ |
阴离子 | SO42-、OH-、CO32-、Cl- |
现进行如下实验:
①足量A溶液与B溶液混合共热可生成沉淀甲和刺激性气味气体;
②少量A溶液与C溶液混合可生成沉淀乙;
③A溶液与B溶液均可溶解沉淀乙,但都不能溶解沉淀甲。
请回答:
(1)A的化学式为_________;室温时,将pH相等的A溶液与D溶液分别稀释10倍,pH分别变为a和b,则a _______b(填“>”、“=”或“<”)。
(2)加热蒸干C溶液并灼烧,最后所得固体为_______(填化学式)。
(3)C溶液与D溶液反应的离子方程式为_______。
(4)向B溶液中逐滴加入等体积、等物质的量浓度的NaOH溶液,滴加过程中水的电离平衡将_______(填“正向”、“不”或“逆向”)移动;最终所得溶液中各离子浓度由大到小的顺序为__________________。
(5)已知沉淀甲的Ksp=x。将0.03mol·L-1的A溶液与0.01mol·L-1的B溶液等体积混合,混合溶液中酸根离子的浓度为_______ (用含x的代数式表示,混合后溶液体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:选择题
下列有关说法正确的是
A、氨水稀释后,溶液中 的值减小
的值减小
B、 0.1 mol·L-1Na2CO3溶液加蒸馏水稀释,CO32-的水解程度增大,溶液的pH减小
C、电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等
D、 298 K时,2H2S(g)+SO2(g)=3S(s)+2H2O(l)能自发进行,则其ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测11 题型:选择题
常温下,向20.00 mL 0.100 mol·L-1 CH3COONa溶液中逐滴加入0.100 0 mol·L-1盐酸,溶液的pH与所加盐酸体积的关系如下图所示(不考虑挥发)。下列说法正确的是
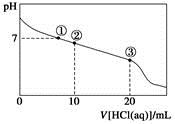
A.点①所示溶液中:c(CH3COOH)=c(Cl-)>c(OH-)=c(H+)
B.点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH)
C.点③所示溶液中:c(CH3COOH)>c(Na+)>c(H+)>c(CH3COO-)
D.整个过程中可能出现:c(H+)+c(Na+)=c(CH3COOH)+c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--预测10 题型:选择题
下列说法正确的是
A.第三周期金属元素的氧化物都属于碱性氧化物
B.电子层结构相同的不同离子,其半径随核电荷数增大而减小
C.IA族元素的金属性一定比IIA族元素的金属性强
D.单原子形成的离子,一定与稀有气体原子的核外电子排布相同
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--线索综合3 题型:简答题
二甲醚(CH3OCH3)是一种重要的清洁燃料气,其储运、燃烧安全性、理论燃烧温度等性能指标均优于液化石油气,也可用作燃烧电池的燃料,具有很好的好展前景。
(1)已知H2、CO和CH3OCH3的燃烧热(ΔH)分别为-285.5kJ/mol、-283kJ/mol和-1460.0 kJ/mol,则工业上利用水煤气成分按1:1合成二甲醚的热化学方程式为: 。
(2)工业上采用电浮远凝聚法处理污水时,保持污水的pH在5.0,通过电解生成Fe(OH)3胶体,吸附不溶性杂质,同时利用阴极产生的H2,将悬浮物带到水面,利于除去。实验室以二甲醚燃料电池模拟该方法设计的装置如下图所示:
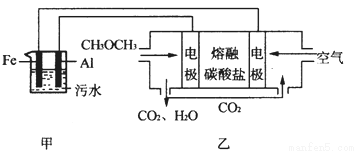
①乙装置以熔融碳酸盐为电解质,稀土金属材料为电极。写出该燃料电池的正极电极反应式 ;下列物质可用做电池熔融碳酸盐的是 。
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)2CO3
②写出甲装置中阳极产物离子生成Fe(OH)3沉淀的离子方程式 。
③已知常温下Ksp[Fe(OH)3]=4.0×10-38,电解一段时间后,甲装置中c(Fe3+)= 。
④已知:H2S的电离平衡常数:K1=9.1×10-8、K2=1.1×10-12;H2CO3的电离平衡常数:K1=4.31×10-7、K2=5.61×10-11。测得电极上转移电子为0.24mol时,将乙装置中生成的CO2通入200mL 0.2mol/L的Na2S溶液中,下列选项正确的是
A.发生反应的离子方程式为:CO2+S2-+H2O=CO32-+H2S
B.发生反应的离子方程式为:CO2+S2-+H2O=HCO3-+HS-
C.c(Na+)=2[c(H2S)+c(HS-)+c(S2-)]
D.c(Na+)+c(H+)=2c(CO32-)+2c(S2-)+c(OH-)
E.c(Na+)>c(HCO3-)>c(HS-)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com