
| A. | NaOH | B. | CaO | C. | 氢氟酸 | D. | H2O |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,则H2的标准燃烧热为-241.8 kJ•mol-1 | |
| B. | 若C(石墨,s)=C(金刚石,s)△H>0,则石墨比金刚石稳定 | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ•mol-1,则20.0g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量 | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨和氯化钠分别受热熔化 | B. | 冰的融化和水的分解 | ||
| C. | NaCl和HCl溶于水 | D. | 干冰和碘的升华 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
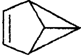 (其中C、H原子已略去),下列关于盆烯的说法中正确的是( )
(其中C、H原子已略去),下列关于盆烯的说法中正确的是( )| A. | 盆烯是乙烯的一种同系物 | |
| B. | 盆烯分子中所有的碳原子可能在同一平面上 | |
| C. | 盆烯是苯的一种同分异构体 | |
| D. | 盆烯在一定条件下可以发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(NO3)2+H2SO4═BaSO4↓+2HNO3 | B. | BaCl2+Na2SO4═BaSO4↓+2NaCl | ||
| C. | Ba(OH)2+K2SO4═BaSO4↓+2KOH | D. | Ba(OH)2+H2SO4═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
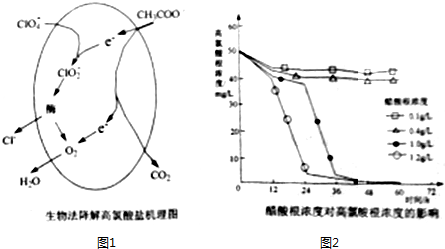
| 酸 | HClO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | 1.6×10-9 | 4.2×10-10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com