
双球连通管中发生2NO2⇌N2O4+Q(Q>0).若同时向两烧杯中分别加入等温、等体积的蒸馏水(左)和0.1mol/L H2O2溶液(右),再向右侧烧杯中加入少量Fe2(SO4)3固体后,则下列有关推断中正确的是( )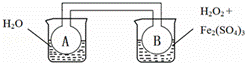
|
| A. | 实验时,A、B中的压强始终相等 |
|
| B. | 若右侧烧杯发生吸热反应,则A中更快达到平衡 |
|
| C. | 若右侧烧杯发生放热反应,则A中颜色较深 |
|
| D. | 能用该装置推断右侧烧杯中反应的热效应 |
| 化学平衡的影响因素. | |
| 专题: | 化学平衡专题. |
| 分析: | A、AB是连通器,实验时AB中压强相同; B、2NO2(红棕色)⇋N2O4(无色),△H<0是放热反应,过氧化氢加入硫酸铁会做催化剂使过氧化氢分解,若右侧烧杯发生吸热反应,则B温度降低反应正向进行,AB中达到平衡; C、2NO2(红棕色)⇋N2O4(无色),△H<0是放热反应,若双氧水的分解反应也是放热反应.当右边双氧水分解时放出的热量会使B瓶升温,使瓶中反应朝逆向反应方向移动,即向生成NO2移动,故B瓶颜色更深; D、依据气体颜色变化分析烧杯中反应的能量变化,若B中气体颜色加深证明是放热反应,变浅证明是吸热反应. |
| 解答: | 解:A、AB是连通器,实验时AB中压强始终相同,故A正确; B、2NO2(红棕色)⇋N2O4(无色),△H<0是放热反应,过氧化氢加入硫酸铁会做催化剂使过氧化氢分解,若右侧烧杯发生吸热反应,则B温度降低反应正向进行,AB中达到相同平衡,故B错误; C、2NO2(红棕色)⇋N2O4(无色),△H<0是放热反应,若双氧水的分解反应也是放热反应.当右边双氧水分解时放出的热量会使B瓶升温,使瓶中反应朝逆向反应方向移动,即向生成NO2移动,故B瓶颜色更深,故C错误; D、若B中气体颜色加深证明是放热反应,变浅证明是吸热反应,可以用该装置推断右侧烧杯中反应的热效应,故D正确; 故选AD. |
| 点评: | 本题考查了化学平衡影响因素分析判断,化学平衡移动原理理解应用,注意反应特征的分析应用,掌握基础是关键,题目难度中等. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
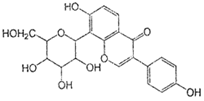
葛根素具有降血压等作用,其结构简式如下图,下列有关说法正确的是( )
A.该物质在一定条件下能发生消去反应、加成反应、取代反应
B.葛根素的分子式为C21H22O9
C.该物质一个分子中含有5个手性碳原子
D.一定条件下1 mol 该物质与H2反应最多能消耗7 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是( )
|
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 |
|
| C. | 铝与Fe2O3发生铝热反应 | D. | 将锌粒投入Cu(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
茶叶中铁元素的检验可经过以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )
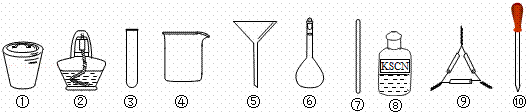
|
| A. | 将茶叶灼烧灰化,选用①、②和⑨ |
|
| B. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ |
|
| C. | 过滤得到的滤液,选用④、⑤和⑦ |
|
| D. | 检验滤液中的Fe3+,选用③、⑧和⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室从含碘废液(除H2O外,还含有CCl4、I2、I﹣)中回收碘,其实验过程如图1:
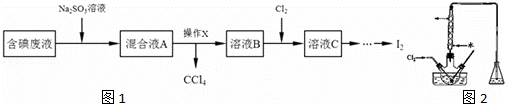
(1)向含碘废液中加入稍过量的Na2SO3溶液时发生的离子方程式为 ;该操作的目的是 .
(2)操作X应在 (填写仪器名称图2)中进行,简述得到溶液B的过程:将混合溶液静置后,
(3)在三颈瓶中将溶液B用盐酸调至pH约为2,缓慢通入Cl2,在40˚C左右反应(实验装置如右图所示).实验控制在较低温度下进行的原因是 ;锥形瓶里盛放的溶液为 (填溶质的化学式).
(4)某含碘废水(pH约为4)中一定存在I2,可能存在I﹣或IO3﹣.可以使用 (填溶质的化学式,下同)溶液检验可能存在的I﹣或 溶液检验可能存在的IO3﹣.在检验该含碘废水中是否含有I﹣或IO3﹣前必需要进行的操作是 (填序号).
a.取适量含碘废水用CCl4多次萃取、分液
b.用NaOH溶液将溶液调节到中性
c.向溶液中滴入少量淀粉溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有较大量的Cl-、CO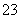 、OH-3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次沉淀出来,下列实验操作顺序正确的是( )
、OH-3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次沉淀出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液
④滴加Ba(NO3)2溶液
A.①②④②③ B.④②①②③
C.①②③②④ D.④②③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式____________________________________________________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为________,其水溶液与F单质反应的化学方程式为____________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显________色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为________;c的电子式为________;d的晶体类型是________。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料。羰基法提纯粗镍涉及的两步反应依次为:
(1)Ni(S)+4CO(g) 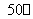 Ni(CO)4(g)+Q
Ni(CO)4(g)+Q
(2)Ni(CO)4(g) 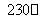 Ni(S)+4CO(g)
Ni(S)+4CO(g)
完成下列填空:
(1)在温度不变的情况下,要提高反应(1)中Ni(CO4)的产率,可采取的措施有 、 。
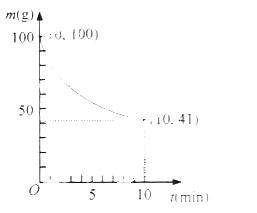
(2)已知在一定条件下的2L密闭容器中制备Ni(CO)4,粗镍(纯度98.5%,所含杂质不与CO反应)剩余质量和反应时间的关系如右图所示。Ni(CO)4在0~10min的平均反应速率为 。
(3)若反应(2)达到平衡后,保持其他条件不变,降低温度,重新达到平衡时 。
a.平衡常数K增大 b.CO的浓度减小
c.Ni的质量减小 d.v逆【Ni(CO)4】增大
(4)简述羰基法提纯粗镍的操作过程。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com