
锌–空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O===2Zn(OH) 。下列说法正确的是
。下列说法正确的是
A.充电时,电解质溶液中K+向阳极移动
B.充电时,电解质溶液中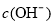 逐渐减小
逐渐减小
C.放电时,负极反应为:Zn+4OH–-2e–===Zn(OH)
D.放电时,电路中通过2mol电子,消耗氧气22.4L(标准状况)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年安徽六安一中高一下周末作业四化学试卷(解析版) 题型:选择题
SF6是一种优良的绝缘气体,分子结构中只存在S—F键。己知:1 mol S (s)转化为气态硫原子吸收能量280kJ,断裂1mol F—F、S—F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g),产生1mol SF6(g)的反应的热量变化为
A.放出1780kJ B.放出1220kJ C.吸收1780kJ D.吸收1220kJ
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(天津卷参考版) 题型:简答题
氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是_________(至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:____________。
(2)氢气可用于制备H2O2。已知:
H2(g)+A(l)=B(l) ΔH1
O2(g)+B(l)=A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+ O2(g)= H2O2(l)的ΔH____0(填“>”、“<”或“=”)。
(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)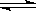 MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
a.容器内气体压强保持不变
b.吸收y mol H2只需1 mol MHx
c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______。
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH? 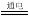 FeO42?+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42?,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
FeO42?+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42?,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
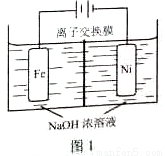
①电解一段时间后,c(OH?)降低的区域在_______(填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______。
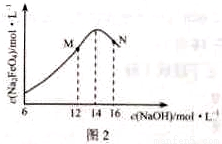
③c( Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c( Na2FeO4)低于最高值的原因:_____________。
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(四川卷参考版) 题型:选择题
NA为阿伏伽德罗常数的值。下列说法正确的是
A.2.4g镁在足量的氧气中燃烧,转移的电子数为0.1NA
B.标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA
C.氢原子数为0.4NA的甲醇分子中含有的σ键数为0.4NA
D.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(全国3卷参考版) 题型:实验题
以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
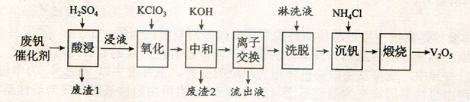
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124?形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124?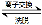 R4V4O12+4OH?(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”“碱”“中”)。
R4V4O12+4OH?(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”“碱”“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(全国2卷参考版) 题型:推断题
[化学--选修5:有机化学基础]
氰基丙烯酸酯在碱性条件下能快速聚合为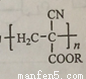 ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
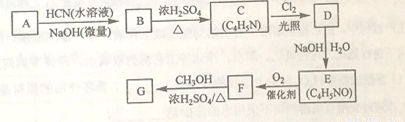
已知:
①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②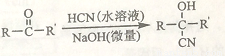
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)由C生成D的反应类型为________。
(4)由D生成E的化学方程式为___________。
(5)G中的官能团有___、 ____ 、_____。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有_____种。(不含立体异构)
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(全国2卷参考版) 题型:选择题
某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水仍有部分固体未溶解;再加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在。
该白色粉末可能为
A.NaHCO3、Al(OH)3 B.AgCl、NaHCO3 C.Na2SO3 、BaCO3 D.Na2CO3、CuSO4
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(全国1卷参考版) 题型:选择题
设NA为阿伏加德罗常数值。下列有关叙述正确的是
A.14 g乙烯和丙烯混合气体中的氢原子数为2NA
B.1 molN2与4 mol H2反应生成的NH3分子数为2NA
C.1 molFe溶于过量硝酸,电子转移数为2NA
D.标准状况下,2.24 LCCl4含有的共价键数为0.4NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州市十校联合高二下期中化学试卷(解析版) 题型:选择题
某同学设计了由乙醇合成乙二醇的路线如下。下列说法正确的是( )
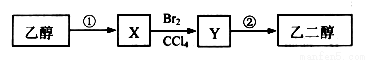
A. X可以发生加成反应
B. 等物质的量的乙醇、X完全燃烧,消耗氧气的量不相同
C. 步骤②需要在氢氧化钠醇溶液中反应
D. 步骤①的反应类型是水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com