
 已知A是灰黑色、有金属光泽的固体单质.根据如图所示的物质之间的转化关系,回答下列有关问题. (1)写出B、C两物质的名称:B硅酸钠,C硅酸.
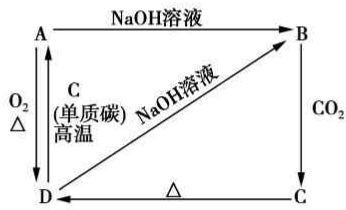
已知A是灰黑色、有金属光泽的固体单质.根据如图所示的物质之间的转化关系,回答下列有关问题. (1)写出B、C两物质的名称:B硅酸钠,C硅酸.分析 A是灰黑色、有金属光泽的固体单质,根据转化关系,A能与氢氧化钠反应,同时由D与碳高温条件下制得,可知A为硅,硅与氧气反应生成D为二氧化硅,硅与氢氧化钠反应生成B为硅酸钠,硅酸钠与二氧化碳反应生成C为硅酸,硅酸受热分解得D为二氧化硅,二氧化硅与氢氧化钠反应生成硅酸钠,符合各物质转化关系,据此答题.
解答 解:A是灰黑色、有金属光泽的固体单质,根据转化关系,A能与氢氧化钠反应,同时由D与碳高温条件下制得,可知A为硅,硅与氧气反应生成D为二氧化硅,硅与氢氧化钠反应生成B为硅酸钠,硅酸钠与二氧化碳反应生成C为硅酸,硅酸受热分解得D为二氧化硅,二氧化硅与氢氧化钠反应生成硅酸钠,符合各物质转化关系,
(1)根据上面的分析可知,B为硅酸钠,C为硅酸,
故答案为:硅酸钠;硅酸;
(2)D→B为二氧化硅与氢氧化钠反应生成硅酸钠,反应的化学方程式为SiO2+2NaOH═Na2SiO3+H2O,
故答案为:SiO2+2NaOH═Na2SiO3+H2O;
(3)B→C为硅酸钠溶液与二氧化碳反应生成硅酸,反应的离子方程式为CO2+SiO32-+H2O═H2SiO3↓+CO32-,
故答案为:CO2+SiO32-+H2O═H2SiO3↓+CO32-.
点评 本题考查硅和二氧化硅的性质和用途,题目难度不大,注意题中各物质的转化关系,为解答该题的关键.


 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 还原性:X->Y- | |
| B. | 在X-、Y-、Z-、W- 中 Z- 的还原性最强 | |
| C. | 氧化性:Z2>W2 | |
| D. | 反应2Z-+Y2=2Y-+Z2可以发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯净物②③⑥ | B. | 混合物①③④ | C. | 电解质②⑥ | D. | 非电解质④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
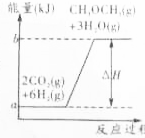 ,工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用进行的,反应器中发生了下列反应:
,工业上制二甲醚是在一定温度(230~280℃)、压强(2.0~10.0MPa)和催化剂作用进行的,反应器中发生了下列反应:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
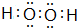 该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”)
该物质能使酸性KMnO4溶液褪色,在这个反应中体现了该物质的还原性(填“氧化性”或“还原性”)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8 | B. | 10 | C. | 12 | D. | 14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 mol | B. | 3.4 mol | C. | 2.8 mol | D. | 1.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
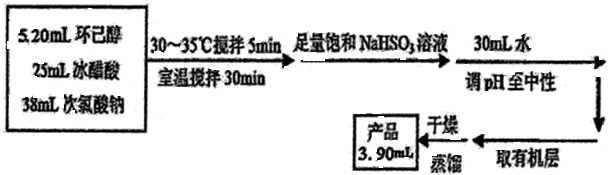
 环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.某化学兴趣小组尝试用次氯酸钠制备环己酮.方程式为:
环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.某化学兴趣小组尝试用次氯酸钠制备环己酮.方程式为: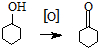
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com