
���ݱ�����Ϣ�жϣ�����ѡ���ȷ���ǣ� ��
| ���� | �μӷ�Ӧ������ | ������ |
| �� | KMnO4 ��H2O2 ��H2SO4 | K2SO4 ��MnSO4���� |
| �� | Cl2 ��FeBr2 | FeCl3��FeBr3 |
| �� | MnO4�� ���� | Cl2 ��Mn2+ ���� |
D
�������������������ԭ��Ӧ����Ҫ������Ԫ�صĻ��ϼ���������������ԭ��Ӧ�Ļ�������ͻ������ɽ�������A����Ӧ��KMnO4��MnSO4��MnԪ�ػ��ϼ���+7�۽���Ϊ+2�ۣ���H2O2����Ԫ�ػ��ϼ����ߣ���������������HԪ���غ��֪������ˮ����ȷ��B���������Ϣ֪����Ӧ��ֻ���������ӱ����������ݵ���ת���غ�2n��C12��=n��FeBr2������n��C12����n��FeBr2��=1��2����ȷ��C���������Ϣ֪��MnO4-����Cl-ΪCl2��ClԪ�ػ��ϼ���-1������Ϊ0�ۣ�����1mo1C12ת�Ƶ���Ϊ2mo1����ȷ��D��������������ǿ���������������ԣ��ɢۿ�֪������MnO4-��Cl2���ɢڿ�֪������Cl2��Fe3+���ɢڿ�֪Fe3+��������Br-��������Br2��Fe3+������
���㣺����������ԭ��Ӧ�Ļ�������ͻ������ɡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�������ײ���MFe2Ox��3��x��4����M��ʾ��2�۵Ľ���Ԫ�أ��ڷ�Ӧ�л��ϼ۲������仯�������£�MFe2Ox��ʹ��ҵ�����е�SO2ת��ΪS���������£�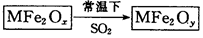
�������ж���ȷ���ǣ� ��
| A��x��y | B��MFe2Ox�ǻ�ԭ�� |
| C��SO2�Ǹ÷�Ӧ�Ĵ��� | D��SO2�������û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ڵ��۵⻯����Һ�м�����������������Һ������Һ�����������жϴ������
| A�������ԣ�ClO����SO42����I2 |
| B��Ư�۾���Һ��ʹ���۵⻯����ֽ���� |
| C��ClO����I���ڼ����������Է���������ԭ��Ӧ |
| D����������ˮ�м�����������������Һ����ˮ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ڷ�Ӧ14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4������˵����ȷ����
| A��ֻ������ͭ�������� |
| B��SO42-�Ȳ������������ֲ��ǻ�ԭ���� |
| C�������������뱻��ԭ�����������Ϊ3��7 |
| D��1mol����ͭ��������5/7mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����ͭ����Ҫ���ջ�ͭ���䷴ӦΪ��2CuFeS2+O2��Cu2S+2FeS+SO2 ����˵����ȷ����
| A��Cu2S���������������ǻ�ԭ���� |
| B��ÿ����1 molCu2S����4mol������ |
| C��CuFeS2������ԭ������Ԫ�ر����� |
| D��ÿת��1.2 mol���ӣ���0��2 mol������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
4 mL 0.5 mol/L��ijKXO4��Һǡ���ܽ�160 mL 0.1 mol/L��FeSO4��������Һ��Ӧ��ȫ����XԪ���ڻ�ԭ�����еĻ��ϼ�Ϊ
| A����1 | B��0 | C����2 | D����3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���й��� NO2�� H2O��Ӧ��˵���У���ȷ����( )��
| A��NO2ֻ�������� | B��NO2ֻ����ԭ�� |
| C��NO2������������������ԭ�� | D��NO2�Ȳ������������ֲ�����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ڷ�Ӧ3Cl2��8 NH3 = N2��6NH4Cl�У��������뻹ԭ�������ʵ���֮��Ϊ�� ��
| A��8:3 | B��3:8 | C��3:2 | D��1:3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ԭ��Ӧ�У�ˮ�����ÿ���������������ԭ�����������������ǻ�ԭ�����ȷ��������ַǻ�ԭ���ȡ����з�Ӧ��Br2+SO2+2H2O=H2SO4+2HBr��Ƚϣ�ˮ�����ò���ͬ���ǣ� ��
| A��2Al+2NaOH+2H2O=2NaAlO2+3H2�� |
| B��4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C��BrCl+H2O=HCl+HbrO |
| D��2Na2O2+2H2O=4NaOH+O2�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com