
近年来,酸雨污染较为严重,防治酸雨成了迫在眉睫的问题。
(1)有人提出了一种利用氯碱工业产品处理含二氧化硫废气的方法,流程如下:
(Ⅰ)将含SO2的废气通入电解饱和食盐水后所得到的溶液中,得NaHSO3溶液。
(Ⅱ)将电解饱和食盐水所得气体反应后制得盐酸。
(Ⅲ)将盐酸加入NaHSO3溶液中,反应所得到的SO2气体回收,生成的NaCl循环利用。
①写出步骤(Ⅰ)反应的化学方程式:_________________________ _____________________________________________________。
②写出步骤(Ⅱ)中电解饱和食盐水的化学方程式:________________ ______________________________________________________________。
③写出步骤(Ⅲ)反应的离子方程式:_____________________________。
(2)还有学者提出利用Fe2+、Fe3+等离子的催化作用,常温下将SO2氧化成SO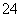 而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO
而实现SO2的回收利用。某研究性学习小组据此设计了如下方案,在实验室条件下测定转化器中SO2氧化成SO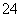 的转化率。
的转化率。

①该小组采用下图装置在实验室测定模拟烟气中SO2的体积分数,X溶液可以是________。(填写序号)
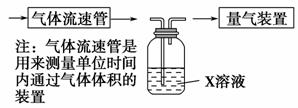
A.碘的淀粉溶液 B.酸性高锰酸钾溶液
C.氢氧化钠溶液 D.氯化钡溶液
②若上述实验是在标准状况下进行的,欲测定转化器中SO2氧化成SO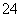 的转化率,已知气体流速,还需测定的数据有____________________________、_________________________。
的转化率,已知气体流速,还需测定的数据有____________________________、_________________________。
解析 求解SO2在混合气中的体积分数,需要求出两个量,一个是SO2的体积,一个是混合气的总体积。利用量气装置,可求出吸收SO2后余气的体积;利用洗气瓶中的X溶液,求出SO2的体积。所以对于洗气瓶中的溶液,必须能与SO2反应,且能发生明显的颜色变化,以便确定反应的终点。求解SO2的转化率,应求出SO2气体的总量和生成SO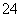 的量。因为在前一问中已求出SO2在混合气中的含量,所以只需确定混合气的总量。利用流速求总量,只需知道通入时间。要求SO2的转化率,只需确定沉淀质量。
的量。因为在前一问中已求出SO2在混合气中的含量,所以只需确定混合气的总量。利用流速求总量,只需知道通入时间。要求SO2的转化率,只需确定沉淀质量。
答案 (1)①SO2+NaOH===NaHSO3
②2NaCl+2H2O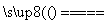 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
③HSO +H+===SO2↑+H2O
+H+===SO2↑+H2O
(2)①A、B ②实验时间 加入盐酸酸化的BaCl2溶液后生成沉淀的质量


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
已知A.B.C.D.E是短周期中原子序数依次增大的5种元素,B.C同周期,D.E也同周期,D原子最外层电子数与最内层电子数相等,A.B.C.D的原子序数之和是E的两倍,D与C形成的化合物是一种耐高温材料,A.B形成的气态化合物的水溶液呈碱性。下列说法正确的是
A.原子半径:D>B>E>C>A B.单质D可用海水作原料获得
C.热稳定性:EA4>A2C D.化合物DC与化合物EC2中化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中,所选装置不合理的是 ( )。
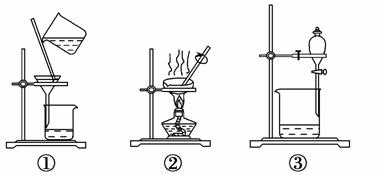
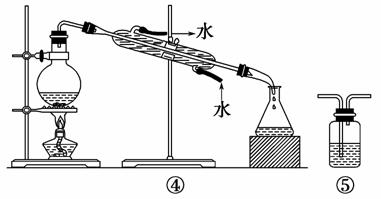
A.分离Na2CO3溶液和CH3COOC2H5,选④
B.用CCl4提取碘水中的碘,选③
C.用FeCl2溶液吸收Cl2选⑤
D.粗盐提纯,选①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
精细化学品具有品种多、批量少、产值高的特点。
(1)表面活性剂在工农业生产和日常生活中广泛应用,其优点是______________,能显著降低水与空气或其他物质的________,提高工业生产________,提高产品的________,故表面活性剂被称为_________________。
(2)在泡沫灭火器中添加表面活性剂可以提高灭火效果的原因是什么?
(3)精细化学品具有特定的功能,特殊的用途,如有些洗衣粉适用于洗衣机,加酶洗衣粉不能用于洗涤____________,医药和农药都有严格的________、__________等。
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验探究课上,同学们积极思考,共设计出如图所示的四种实验方案用以验证浓硫酸的吸水性,其中在理论上可行的是 ( )。
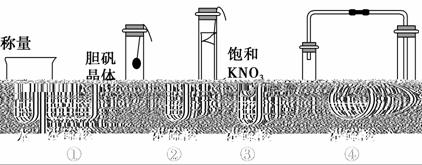
A.①②③④ B.仅①③④
C.仅①②④ D.仅②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家预测,氨有望取代氢能,成为重要的新一代绿色能源。下列有关说法不正确的是 ( )。
A.液氨作为清洁能源的反应原理是4NH3+5O2 4NO+6H2O
4NO+6H2O
B.液氨具有腐蚀性和毒性,在使用过程中要防止液氨泄漏
C.氨气比空气密度小,标准状况下密度约为0.76 g·L-1
D.氨气与氢气相比,优点在于氨气不容易发生爆炸,使用时更安全
查看答案和解析>>
科目:高中化学 来源: 题型:
一定体积0.01 mol·L-1的稀硝酸恰好能氧化一定质量的铁、铝混合物,已知两种金属均被氧化为最高价态,还原产物只有NO。若用0.01 mol·L-1 NaOH溶液溶解相同质量的该混合物,当反应完全时所需氢氧化钠溶液的体积是稀硝酸的 ,则样品中铁、铝的物质的量之比为 ( )。
,则样品中铁、铝的物质的量之比为 ( )。
A.2∶3 B.1∶3
C.1∶4 D.5∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分元素的原子结构特点如表:
| X | L层电子数是K层电子数的3倍 |
| Y | 核外电子层数等于原子序数 |
| Z | L层电子数是K层和M层电子数之和 |
| W | 共用三对电子形成双原子分子,常温下为气体单质 |
(1)画出W原子结构示意图____________________________________。
(2)元素X与元素Z相比,非金属性较强的是______________________,
写出一个能表示X、Z非金属性强弱关系的化学反应方程式__________ ______________________________________________________________。
(3)X、Y、Z、W四种元素形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为__________。
(4)元素X和元素Y以原子个数比1∶1化合形成的化合物Q,元素W和元素Y化合形成的化合物M,Q和M的电子总数相等。以M为燃料,Q为氧化剂,可作火箭推进剂,最终生成无毒的,且在自然界中稳定存在的物质,写出该反应的化学方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
烯烃A在一定条件下可以按下图进行反应
已知:CH3CH2CH2CH2CH2CH2Br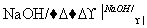 CH3CH2CH2CH2CH===CH2
CH3CH2CH2CH2CH===CH2
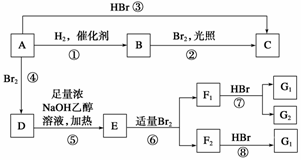
已知D为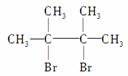 ,F1和F2互为同分异构体,G1和G2互为同分异构体。
,F1和F2互为同分异构体,G1和G2互为同分异构体。
请填空:
(1)A的结构简式是
________________________________________________________________________。
(2)框图中属于取代反应的是(填数字代号):__________________。
(3)框图中属于加成反应的是__________________。
(4)写出D―→E的化学方程式
________________________________________________________________________。
(5)G1的结构简式是
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com