


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源:不详 题型:填空题
 xFe2O3的铝灰制备Al2(S04)3
xFe2O3的铝灰制备Al2(S04)3 18H2O,工艺流程如下:
18H2O,工艺流程如下: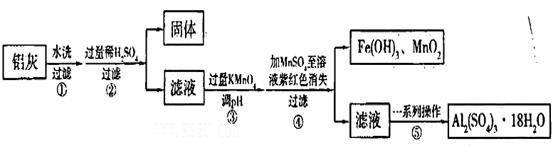
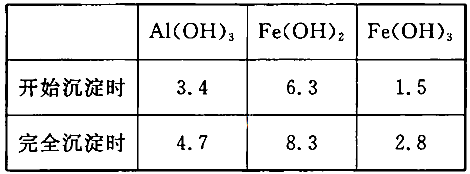
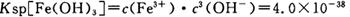 当pH=2时,Fe3+开始沉淀的浓度为_______________。
当pH=2时,Fe3+开始沉淀的浓度为_______________。| A.蒸发皿 | B.坩埚 | C.玻璃棒 | D.酒精灯E.漏斗 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.全部 | B.①②③ |
| C.①②③⑤ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 样品甲 | 生成白色沉淀,继续滴加氢氧化钠溶液,沉淀消失 |
| 样品乙 | 生成白色沉淀,白色沉淀迅速变为灰绿色,最终变为红褐色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
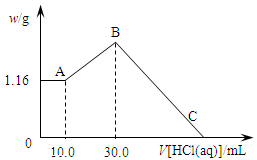
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铝在常温下不能与氧气反应 | B.铝不能与氯气反应 |
| C.氧化铝只能与酸反应,不能与碱反应 | D.铝既能溶于酸,又能溶于强碱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 现象或反应 | 原理解释 |
| A. | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔对熔化的铝有较强的吸附作用 |
| B. | 合成氨反应需在高温条件下进行 | 该反应为吸热反应 |
| C. | 镀层破损后,镀锡铁比镀锌铁易腐蚀 | 锡比锌活泼 |
| D. | 2CO=C+O2在任何条件下均不能自发进行 | 该反应△H>0,△S<0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.①③⑤ | C.①③④⑤ | D.①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com