
【题目】下列物质中属于强电解质的是 ( )
A. NH3·H2O B. H2O C. CH3COOH D. CH3COONH4
科目:高中化学 来源: 题型:
【题目】下列反应中生成物总能量高于反应物总能量的是
A.氢氧化钠溶液与稀硫酸混合 B.异丁醇燃烧
C.氢氧化钡晶体与氯化铵晶体混合搅拌 D.氧化钙溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
(1)Ca(OH)2悬浊液与H2O2溶液反应可制备CaO2·8H2O。
Ca(OH)2+H2O2+6H2O![]() CaO2·8H2O反应时通常加入过量的Ca(OH)2,其目的是 。
CaO2·8H2O反应时通常加入过量的Ca(OH)2,其目的是 。
(2)向池塘水中加入一定量的CaO2·8H2O后,池塘水中浓度增加的离子有____________(填序号)。
A.Ca2+ B.H+ C.CO32- D.OH
(3)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置,加入适量稀H2SO4,等MnO(OH)2与I完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
O2![]() MnO(OH)2
MnO(OH)2 ![]() I2
I2 ![]() S4O62
S4O62
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式 ;
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧为 mg·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.H2(g)+Br2(g)=2HBr(g) ΔH=-72 kJ·mol-1其他相关数据如下表:

则表中a为230
B.已知:H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3kJ·mol-1
所以![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)=
Ba(OH)2(aq)=![]() BaSO4(s)+H2O(l)ΔH=-57.3kJ·mol-1
BaSO4(s)+H2O(l)ΔH=-57.3kJ·mol-1
C.已知CH4(g)+2O2(g)=CO2(g)+2H2O(g)ΔH=-802.33kJ·mol-1,则CH4的燃烧热为802.33kJ·mol-1
D.已知2C(s)+2O2(g)=2CO2(g)ΔH1,2C(s)+O2(g)=2CO(g)ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g) ![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为___________反应(填“吸热”或“放热”),且m+n____________p(填“>”“=”“<”)。
(2)减压使容器体积增大时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(维持体积不变),则A的转化率_________。
(4)若升高温度,则平衡时B、C的浓度之比![]() 将_________。
将_________。
(5)若加入催化剂,平衡时气体混合物的总物质的量____ _____。
(6)若B是有色物质,A、C均无色,则加入C(容器体积不变)时混合物颜色______ _;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俄罗斯用“质子﹣M”号运载火箭成功将“光线”号卫星送入预定轨道。发射用的运载火箭使用的是以液氢为燃烧剂,液氧为氧化剂的高能低温推进剂,已知:
(1)H2(g)=H2(l)△H1=﹣0.92kJmol﹣1
(2)O2(g)=O2(l)△H2=﹣6.84kJmol﹣1
(3)如图:下列说法正确的是( )
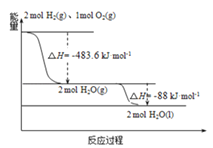
A. 2mol H2(g)与1mol O2(g)所具有的总能量比2molH2O(g)所具有的总能量低
B. 氢气的燃烧热为△H=﹣241.8 kJmol﹣1
C. 火箭液氢燃烧的热化学方程式2H2(l)+O2(l)═2H2O(g)△H=﹣474.92kJmol﹣1
D. H2O(g)变成H2O(l)的过程中,断键吸收的能量小于成键放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大。A与D同主族,可形成DA型离子化合物,B与C同周期且相邻,C与E同主族,E2-与Ar原子具有相同的电子层结构,W的合金用量最大、用途最广。请回答下列问题:
(1)W元素在元素周期表中的位置为 。
(2)下列说法正确的是( )
A.原子半径:A<B<C<D<E
B.D2WC4可以用来做消毒剂和净水剂
C.A4B2C3中既含有离子键又含有共价键
D.D2C2与EC2可以反应生成D2EC3和C2
(3)灼热的碳能与B的最高价氧化物对应水化物的浓溶液反应,化学反应方程式为 。
(4)向盛有A2C2溶液的试管中加入几滴酸化的WEC4溶液,溶液变成棕黄色,发生反应的离子方程式为 ;一段时间后,溶液中有大量气泡出现,随后溶液温度升高,有红褐色沉淀生成,则产生气泡的原因是 ;生成沉淀的原因是 (用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 mL A12(S04)3 溶液中,含 Al3+为 1.62 g,在该溶液中加入 0.1 molL-1 Ba(OH)2溶液100 mL,反应后溶液中SO42-的物质的量浓度约为
A.0.4 molL-1 B.0.3molL-1 C.0.2 molL-1 D.0.1 molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在FeCl3和CuCl2的混和溶液中,加入过量Fe粉,完全反应后,余下固体的质量与所加Fe粉质量相等,则原混和液中FeCl3和CuCl2的物质的量浓度之比为( )
A.7:2 B.2:7 C.1:2 D.2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com