
 �ñ�ǩ��ʾŨ��������250mL 0.4mol/L��ϡ���ᣬ�������й�ʵ�飮��ش�
�ñ�ǩ��ʾŨ��������250mL 0.4mol/L��ϡ���ᣬ�������й�ʵ�飮��ش����� ��1������C=$\frac{1000�Ѧ�}{M}$����Ũ��������ʵ���Ũ�ȣ�������Һϡ���������ʵ����ʵ������������ҪŨ���������
��2����������һ�����ʵ���Ũ����Һһ�㲽��ѡ����Ҫ������
��3���������������ʵ����ʵ�������Һ�����Ӱ�죬����C=$\frac{n}{V}$������������
��4������Na2CO3+2HCl=2NaCl+H2O+CO2�� NaHCO3 +HCl=NaCl+H2O+CO2������������غ������
��� �⣺��1��Ũ��������ʵ���Ũ��C=$\frac{1000��1.18��36.5%}{36.5}$=11.8mol/L������ҪŨ�������ΪV��������Һϡ���������ʵ����ʵ�������ã�V��11.8mol/L=250mL��0.4mol/L�����V=8.5mL��
�ʴ�Ϊ��8.5��
��2������һ�����ʵ���Ũ����Һһ�㲽�裺���㡢��ȡ��ϡ�͡���ȴ����Һ��ϴ�ӡ����ݵȣ��õ�����������Ͳ����ͷ�ιܡ��ձ�����������250mL����ƿ���������õ�����������ͷ�ι� 250mL����ƿ��
�ʴ�Ϊ����ͷ�ιܣ�250mL����ƿ��
��3��A������ʱ���ӿ̶��ߣ�������Һ���ƫС����ҺŨ��ƫ�ͣ�
B������ƿ�ڱڸ���ˮ���δ���ﴦ���������ʵ����ʵ�������Һ�����������Ӱ�죬��ҺŨ�Ȳ��䣻
�ʴ�Ϊ�����䣻
C���ܽ��û����ȴ����ж��ݣ���ȴ����Һ���ƫС����ҺŨ��ƫ�ߣ�
�ʴ�Ϊ��ƫ�ߣ�
��4������Na2CO3��NaHCO3������ֱ�ΪXmol��Ymol����
106X+84Y=5.92��
��250mL 0.4mol/L��ϡ���ᣬ���Ȼ����������Ϊ��0.4mol/L��0.25L=0.1mol��
���ݷ���ʽ��Na2CO3+2HCl=2NaCl+H2O+CO2�� NaHCO3 +HCl=NaCl+H2O+CO2����̼���ƣ�̼��������ȫ��Ӧ�����Ȼ��ƣ�������ԭ�Ӹ����غ㣬��֪�����Ȼ������ʵ���Ϊ0.1mol��
��2X+Y=0.1��
106X+84Y=5.92��
2X+Y=0.1��
��ã�Y=0.02��X=0.04��
��̼���Ƶ�����������$\frac{106g/mol��0.04mol}{5.92g}$��1005=71.6%
�ʴ�Ϊ��71.6%��
���� ���⿼����һ�����ʵ���Ũ����Һ�����ƣ��йط���ʽ�ļ��㣬��ȷ��Һ���Ʋ��輰�����ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ӧ���ʵ���Ҫ������Ũ�ȡ�ѹǿ���¶� | |
| B�� | ����ƿ����Ͳ���ζ����϶�����ʹ���¶ȣ�����ƿ�ޡ�0���̶ȣ���Ͳ���ζ����С�0���̶ȣ�ʵ��ʱ�ζ���ˮϴ������ϴ��������ƿˮϴ������ϴ | |
| C�� | Ϊʵ�鰲ȫ���������и������ı������ʷ�Ӧ�Ż�ԭ�Լ�ƿ����������ĥ����ػ������ | |
| D�� | ������Ӧ������Ļ��Һ�м��뱥��ʳ��ˮ����ͨ����Һ���������Ӳ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
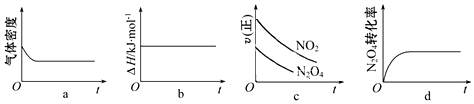
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ��������ԭ��Ӧ | |
| B�� | �÷�Ӧ�ġ�H��0 | |
| C�� | ���������ʵĻ�ѧʽΪ Fe2S3 | |
| D�� | ���������ʵ����������ڷ�Ӧ�����ۺ���۵������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڶ��ױ���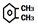 �������ǻ�����ȩ�� �������ǻ�����ȩ��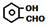 ���۷е�������Ӧ��λȡ���� ���۷е�������Ӧ��λȡ���� | |
| B�� | ±��Ԫ�صĵ��ʼ����⻯����۷е���ԭ�Ӱ뾶����������� | |
| C�� | ʯī�����ʯ��̼���衢����衢���ס�ˮ���ɱ��۷е����ν��� | |
| D�� | NaCl��MgCl2��MgO��Al2O3�۷е����μ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ʵ�鲽�� | ʵ������ | ���� |
| �� | �������������и�����10mL��ˮ��������ͬȼ���������ֱ����Ҵ���������Ϊȼ�Ͻ��м��ȣ���¼�ӿ�ʼ��ˮ���ڵ�ʱ�䣮 | ���Ҵ����Ⱥ�ʱ118s�������ͼ��Ⱥ�ʱ56s�� | ����2������ ������������������� |
| �� | ʵ���ֹͣ���Ⱥ�ȡ�������۲�������ĵײ��� | ���Ҵ����ȵ�������ײ�ֻ�м�����̿�ڣ��������ͼ��ȵ�������ײ��д�����̿�ڣ� | ����1�������ɷ����ϸ���д�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com