
| A. | 铜、石墨均能导电,所以它们均是电解质 | |
| B. | NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质 | |
| C. | 将25gCuSO4.5H2O晶体加水配成100mL溶液,该溶液的物质的量浓度为1mol/L | |
| D. | 实验室要用容量瓶配制0.2mol/L的NaCl溶液950mL,应称量NaCl固体11.1g |
分析 在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液和熔融状态下都不能导电的化合物为非电解质,无论电解质和非电解质,都一定为化合物,单质和混合物一定不是电解质和非电解质,据此进行解答AB;
C、根据n=$\frac{m}{M}$计算25g CuSO4•5H2O的物质的量,根据c=$\frac{n}{V}$计算溶液中CuSO4的物质的量浓度;
D、实验室无950mL容量瓶,需要1000mL容量瓶,据此计算需要固体的质量.
解答 解:A、铜、石墨属于单质,既不是电解质也不是非电解质,故A错误;
B、NH3、CO2的水溶液导电的原因是一水合氨、碳酸电离出的离子,不是NH3、CO2本身电离的离子,因此NH3、CO2属于非电解质,故B错误;
C、25g CuSO4•5H2O的物质的量为$\frac{25g}{250g/mol}$=0.1mol,故n(CuSO4)=0.1mol,溶液体积为100mL,故该溶液中CuSO4的物质的量浓度为:$\frac{0.1mol}{0.1L}$=1mol/L,故C正确;
D、没有950ml的容量瓶,应选择1000ml容量瓶,配制0.2mol/L的NaCl溶液需氯化钠质量为1L×0.2mol/L×58.5g/mol=11.7g,故D错误,故选C.
点评 本题考查了电解质与非电解质的判断,有关物质的量的有关计算等,题目难度不大,注意掌握电解质与非电解质的概念及区别,明确电解质、非电解质都一定为化合物,质和混合物一定不是电解质和非电解质.


科目:高中化学 来源: 题型:填空题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 硅、二氧化硅、硅酸钠是工业上制造光导纤维的主要原料 | |
| B. | 甘油不是油,油脂不是酯 | |
| C. | 煤的液化、石油分馏都是物理变化 | |
| D. | 废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2L | B. | 33.6L | C. | 22.4L | D. | 6.72L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C+H2O=CO+H2;△H=+131.2KJ/mol | |
| B. | CO(g)+H2(g)=C(s)+H2O(g);△H=-131.2KJ/mol | |
| C. | C(s)+H2O(g)=CO(g)+H2(g);△H=+10.93KJ/mol | |
| D. | C(s)+H2O(g)=CO(g)+H2(g);△H=-131.2KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
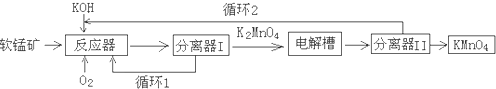
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
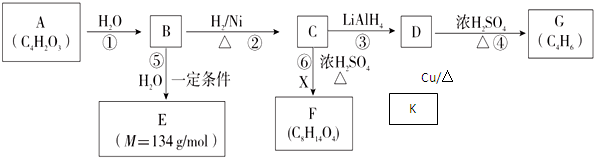
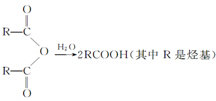 ②R-COOH$\stackrel{LiAlH_{4}}{→}$R-CH2OH(其中R是烃基)
②R-COOH$\stackrel{LiAlH_{4}}{→}$R-CH2OH(其中R是烃基)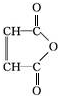 ;B中含氧官能团的名称是羧基;
;B中含氧官能团的名称是羧基;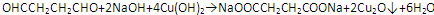
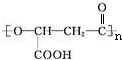 .有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构可有2 种.
.有机物Y与E互为同分异构体,且具有相同的官能团种类和数目,则Y的结构可有2 种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com