

| 实验操作 | 实验现象 | 实验结论 |
| 1 | 2 | 裴置B中的溶液还含有氢氧化钠 |
| 3 | 4 |
分析 (1)根据仪器的特征以及常见仪器的名称解答;
(2)D中盛放的物质过氧化钠,与CO2和水反应,产生O2;
(3)大理石与稀盐酸反应,生成氯化钙,二氧化碳和水;
(4)由实验装置可知,本实验首先由CaCO3和盐酸反应生成CO2,反应生成的二氧化碳中含有氯化氢和水蒸气杂质气体,产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后通过过氧化钠与CO2和水反应,产生O2,用NaOH溶液吸收未反应的二氧化碳,用排水法收集O2,据此选择顺序;
(5)试管N中收集满气体后.下一步实验操作是证明试管中收集的气体是氧气;
(6)二氧化碳和氢氧化钠反应生成碳酸钠和水,氢氧化钠溶液呈碱性,能使酚酞试液变红进行解答,碳酸钠溶液与氯化钡溶液反应生成了碳酸钡和氯化钠,其中碳酸钡为固体,而氯化钠为中性溶液,所以为了确认氢氧化钠是否存在,应该加入过量的氯化钡溶液,然后再取上层清液,加入酚酞溶液进行判断即可.
解答 解:(1)仪器M具有球形的漏斗,带有玻璃活塞,为分液漏斗,
故答案为:分液漏斗;
(2)D中盛放的物质过氧化钠,通过过氧化钠与CO2和水反应,产生O2,
故答案为:过氧化钠;
(3)用稀盐酸与大理石反应,反应的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O,离子反应为:CaCO3+2H+=Ca2++H2O+CO2↑,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(4)装置A:由CaCO3和盐酸反应生成CO2,反应生成的二氧化碳中含有氯化氢和水蒸气杂质气体,装置C:产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,装置D:通过过氧化钠与CO2和水反应,产生O2,装置B:NaOH溶液吸收未反应的二氧化碳,装置E:用排水法收集O2,所以顺序为:ACDBE,
故答案为:ACDB;
(5)本实验的目的为证明过氧化钠可作供氧剂,收集气体后要验证是否为氧气,为防止倒吸,应先把E中的导管移出水面,然后关闭分液漏斗活塞,用带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气,
故答案为:把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气;
(6)取少量样品加水溶解,取少量待测液于试管,加入足量氯化钡溶液至不再产生白色沉淀,再向静置后的上述试管中,滴加少量酚酞溶液;如果溶液没有变红,则说明氢氧化钠完全变质,已经没有氢氧化钠;如果溶液变红,则说明还含有氢氧化钠,
故答案为:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量样品加水溶解,取少量待测液于试管,加入足量氯化钡溶液 | 产生白色沉淀 | 裴置B中的溶液还含有氢氧化钠 |
| 再向静置后的上述试管中,滴加少量酚酞溶液 | 溶液变红 |
点评 本题以钠的化合物为载体综合考查学生的分析能力和实验能力,为高频考点,把握实验的原理和注意事项、实验装置的作用为解答的关键,难度中等.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:选择题
| A. | 通入HCl气体之前:c(S2-)>c(OH-)>c(HS-)>c(H+) | |
| B. | c(Cl-)=0.100mol•L-1的溶液中:c(OH-)-c(H+)=c(H2S)-c(S2-) | |
| C. | pH=7的溶液中:c(Cl-)═c(HS-)+c(H2S) | |
| D. | c(HS-)=c(S2-)的碱性溶液中:c(Cl-)+c(HS-)<0.100mol•L-1+c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO发生氧化反应 | B. | NO2是还原剂 | C. | CO是氧化剂 | D. | N元素化合价升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH3具有还原性 | B. | N2只具有还原性 | C. | N2只具有氧化性 | D. | HNO3具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28 g N2和28 g CO所含的分子数都是NA | |
| B. | 2 g H2和2g O2所含的原子数都是NA | |
| C. | 28 g CO和44 g CO2所含的氧原子数都是2NA | |
| D. | 98 g H2SO4和98 g H3PO4所含的氧分子数都是4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
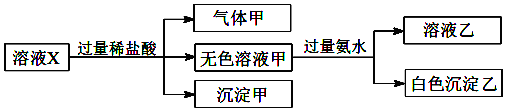
| A. | 气体甲一定是纯净物 | |
| B. | 沉淀甲是硅酸和硅酸钙的混合物 | |
| C. | CO32-和SO42-一定不存在于溶液X中 | |
| D. | Na+、[Al(OH)4]-和SiO32-一定存在于溶液X中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热时,二者均能稳定存在 | B. | 两者均有丁达尔效应 | ||
| C. | 加入盐酸先沉淀,后溶解 | D. | 分散质微粒可通过滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水和氯化铵的pH=7的混合溶液中:c(Cl-)=c(NH4+) | |
| B. | pH=1的一元酸和pH=13的一元碱等体积混合:c(OH-)=c(H+) | |
| C. | 0.1mol•L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) | |
| D. | 0.1mol•L-1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素原子的最外层电子数等于元素的最高化合价 | |
| B. | 只含共价键的物质一定是共价化合物 | |
| C. | P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 | |
| D. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com