

 £®
£®·ÖĪö M”¢NĪŖÉś»īÖŠ³£¼ūµÄ½šŹōµ„ÖŹ£¬NµÄŃõ»ÆĪļŹĒÄĶ»š²ÄĮĻ£¬Ņ²ŹĒŅ±Į¶NµÄŌĮĻ£¬Ńõ»ÆĀĮČŪµćøߣ¬æÉ×÷ÄĶ»š²ÄĮĻ£¬µē½āŃõ»ÆĀĮæɵĆĀĮ£¬ŌņNŹĒĀĮ£¬ĮŖĻµĀĮČČ·“Ó¦æÉÖŖMŹĒĢś£¬EŹĒŃõ»ÆĢś£¬GŹĒĒāŃõ»ÆĢś£¬DĪŖĪŽÉ«ĘųĢ壬ŌŚæÕĘųÖŠ»į³öĻÖŗģ×ŲÉ«£¬ŌņDĪŖNO£¬ĖłŅŌAŹĒFe£ØNO3£©2£¬øł¾ŻĄ¶É«³ĮµķÖŖXŹĒCu£ØNO3£©2£¬FŹĒNa2O2£¬HŹĒŃõĘų£¬BŹĒĀČ»ÆĢś£¬CŹĒCu£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗM”¢NĪŖÉś»īÖŠ³£¼ūµÄ½šŹōµ„ÖŹ£¬NµÄŃõ»ÆĪļŹĒÄĶ»š²ÄĮĻ£¬Ņ²ŹĒŅ±Į¶NµÄŌĮĻ£¬Ńõ»ÆĀĮČŪµćøߣ¬æÉ×÷ÄĶ»š²ÄĮĻ£¬µē½āŃõ»ÆĀĮæɵĆĀĮ£¬ŌņNŹĒĀĮ£¬ĮŖĻµĀĮČČ·“Ó¦æÉÖŖMŹĒĢś£¬EŹĒŃõ»ÆĢś£¬GŹĒĒāŃõ»ÆĢś£¬DĪŖĪŽÉ«ĘųĢ壬ŌŚæÕĘųÖŠ»į³öĻÖŗģ×ŲÉ«£¬ŌņDĪŖNO£¬ĖłŅŌAŹĒFe£ØNO3£©2£¬øł¾ŻĄ¶É«³ĮµķÖŖXŹĒCu£ØNO3£©2£¬FŹĒNa2O2£¬HŹĒŃõĘų£¬BŹĒĀČ»ÆĢś£¬CŹĒCu£®
£Ø1£©XµÄ»ÆѧŹ½ĪŖXŹĒCu£ØNO3£©2£¬MĪŖFe£¬ŌŚÖÜĘŚ±ķÖŠĪ»ÖĆ£ŗµŚĖÄÖÜĘŚµŚ¢ų×壻FŹĒNa2O2£¬µē×ÓŹ½ĪŖ  £¬
£¬
¹Ź“š°øĪŖ£ŗCu£ØNO3£©2£»µŚĖÄÖÜĘŚµŚ¢ų×壻 £»
£»
£Ø2£©·“Ó¦¢ŚµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ3Fe2++NO3-+4H+ØT3Fe3++NO”ü+2H2O£¬
·“Ó¦¢ŪµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ2Al+Fe2O3$\frac{\underline{\;øßĪĀ\;}}{\;}$Al2O3+2Fe£¬
·“Ó¦¢ŪŌŚ¹¤ŅµÉś²śÖŠµÄÓĆĶ¾£ŗŗø½ÓøÖ¹ģ»ņŅ±Į¶ÄŃČŪ½šŹō£¬
M2+ÓėF°“ĪļÖŹµÄĮæÖ®±Č2£ŗ3·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Fe2++3Na2O2+4H2OØT2Fe£ØOH£©3+2OH-+O2”ü+6Na+£¬
¹Ź“š°øĪŖ£ŗ3Fe2++NO3-+4H+ØT3Fe3++NO”ü+2H2O£»2Al+Fe2O3$\frac{\underline{\;øßĪĀ\;}}{\;}$Al2O3+2Fe£»ŗø½ÓøÖ¹ģ»ņŅ±Į¶ÄŃČŪ½šŹō£»2Fe2++3Na2O2+4H2OØT2Fe£ØOH£©3+2OH-+O2”ü+6Na+£»
£Ø3£©ÉčFeµÄÖŹĮæĪŖm£¬Ōņ£ŗ
Fe”«Cu2+”«Cu ¹ĢĢåŌöÖŲ”÷m
56 1mol 64 ””8
m 10.16g-10g=0.16g
ĖłŅŌm=$\frac{0.16g”Į56}{8}$=1.12g
¹ŹĻõĖįŃĒĢśµÄĪļÖŹµÄĮæÅضČĪŖ$\frac{\frac{1.12g}{56g/mol}}{0.1L}$=0.2mol/L£¬
¹Ź“š°øĪŖ£ŗ0.2mol/L£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļĶʶĻ£¬ĪļÖŹµÄŠŌÖŹ”¢ÓĆĶ¾¼°ŃÕÉ«ŹĒĶʶĻĶ»ĘĘæŚ£¬ŹģĮ·ÕĘĪÕŌŖĖŲ»ÆŗĻĪļŠŌÖŹ£¬£Ø3£©ÖŠ×¢ŅāĄūÓĆ²īĮæ·Ø¼ĘĖć½ā“š£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH3OHµÄČ¼ÉÕČČĪŖ1452kJ•mol-1 | |
| B£® | 2H2£Øg£©+O2£Øg£©ØT2H2O£Øg£©”÷H£¾-571.6kJ•mol-1 | |
| C£® | 2CH3OH£Øl£©+O2£Øg£©ØT2CO2£Øg£©+4H2£Øg£©”÷H=-880.4kJ•mol-1 | |
| D£® | CH3COOH£Øaq£©+NaOH£Øaq£©ØTH2O£Øl£©+CH3COONa£Øaq£©”÷H=-57.3kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ÅØĮņĖįÕ“µ½Ę¤·ōÉĻŹ±£¬æÉĮ¢æĢÓĆ“óĮæµÄĖ®³åĻ“£¬Č»ŗóŌŁĶæÉĻ3%”«5%µÄNaHCO3ČÜŅŗ | |
| B£® | Č”ÓĆ»ÆѧŅ©Ę·Ź±£¬Ó¦ĢŲ±š×¢Ņā¹Ū²ģŅ©Ę·°ü×°ČŻĘ÷ÉĻµÄ°²Č«¾ÆŹ¾±źÖ¾ | |
| C£® | ·²ŹĒøų²£Į§ŅĒĘ÷¼ÓČČ£¬¶¼ŅŖ¼ÓµęŹÆĆŽĶų£¬ŅŌ·ĄŅĒĘ÷ÕØĮŃ | |
| D£® | ĪÅČĪŗĪ»ÆѧŅ©Ę·µÄĘųĪ¶¶¼²»Äܽ«±Ē×Ó“Õ½üŅ©Ę· |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øųŹŌ¹ÜĄļµÄŅŗĢå¼ÓČČ£¬ŅŗĢåµÄĢå»żŅ»°ć²»³¬¹żŹŌ¹ÜČŻ»żµÄ$\frac{1}{2}$ | |
| B£® | Ļņ¾Ę¾«µĘĄļĢķ¼Ó¾Ę¾«£¬²»æɳ¬¹ż¾Ę¾«µĘČŻ»żµÄ$\frac{2}{3}$ | |
| C£® | ¾Ę¾«µĘŹ¹ÓĆĶź±Ļ£¬Ó¦Į¢¼“ÓĆ×ģ“µĆš»šŃę | |
| D£® | ÓĆČ¼×ÅµÄ¾Ę¾«µĘČ„µćČ¼ĮķŅ»Õµ¾Ę¾«µĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
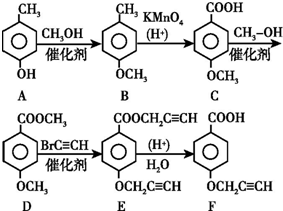
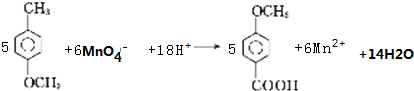 £®
£®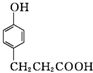 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5ÖÖ | B£® | 4ÖÖ | C£® | 3ÖÖ | D£® | 2ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōĢśÓė¹żĮæµÄĻ”ŃĪĖį·“Ó¦£ŗ2Fe+6H+”ś2Fe3++3H2”ü | |
| B£® | ĀČ»ÆŃĒĢśČÜŅŗÖŠĶØČėÉŁĮæĀČĘų£ŗFe2++Cl2”śFe3++2Cl- | |
| C£® | Ńõ»ÆĀĮÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£ŗAl2O3+2OH-=2AlO2-+H2O | |
| D£® | ĀČ»ÆĀĮČÜŅŗÖŠ¼ÓČė¹żĮæµÄ°±Ė®£ŗAl3++3OH-”śAl£ØOH£©3”ż |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com