
| A. | 在加热条件下能使不活泼金属铜溶解,表现出浓硫酸的强氧化性和酸性 | |
| B. | 可以用铁制或铝制容器贮运,表现出浓硫酸有稳定的化学性质 | |
| C. | 能使胆矾晶体由蓝色变为白色,表现出浓硫酸的脱水性 | |
| D. | 能使蔗糖炭化,表现出浓硫酸的吸水性 |
分析 A.依据铜与浓硫酸反应产物及反应中硫酸中硫元素化合价变化判断;
B.浓硫酸具有强的氧化性;
C.浓硫酸能够吸收晶体中结晶水;
D.浓硫酸能够使有机物中H、O按照2:1生成水,为浓硫酸的脱水性.
解答 解:A.铜与浓硫酸在加热条件下生成硫酸铜,二氧化硫和水,硫元素化合价部分降低,部分不变,所以表现出浓硫酸的强氧化性和酸性,故A正确;
B.浓硫酸具有强的氧化性,能够使铁、铝在常温下钝化,阻止反应进行,可以用铁制或铝制容器贮运,故B错误;
C.能使胆矾晶体由蓝色变为白色,表现出浓硫酸的吸水性,故C错误;
D.能使蔗糖炭化,表现出浓硫酸的脱水性,故D错误;
故选:A.
点评 本题考查了浓硫酸的性质,熟悉浓硫酸性质是解题关键,注意浓硫酸吸水性与脱水性的区别,题目难度不大.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:选择题
| 操作 | 现象 | 结论解释 | |
| A | 过量铁粉加稀硝酸充分反应,滴入KSCN溶液 | 产生红色溶液 | 稀HNO3将铁氧化成Fe3+ |
| B | 某实验小组从资料上获得信息:Fe3+可以氧化银单质.他们用这种方法清洗一批作了银镜反应的试管,配制了Fe3+浓度相同的FeCl3溶液和Fe2(SO4)3溶液,分别用于清洗实验. | 用FeCl3溶液清洗比Fe2(SO4)3溶液清洗得干净 | 他们认为Fe3+氧化银单质的过程可能是一个可逆过程:Fe3++Ag?Fe2++Ag+ |
| C | 苯酚钠溶液中通入少量CO2气体 | 溶液变浑浊 | 碳酸酸性强于苯酚,溶液中还有Na2CO3生成 |
| D | 相饱和碳酸钠溶液通过量CO2气体 | 产生沉淀 | 因为析出Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
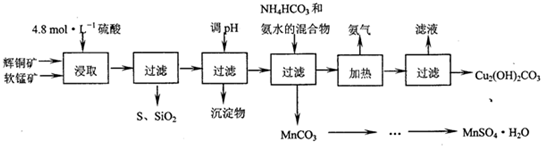
| 开始沉淀的PH | 沉淀完全的PH | |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
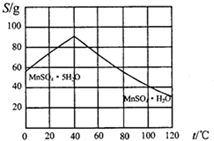
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHS03溶液显酸性:HS03-═H++S032- | |
| B. | 苯酚钠溶液中通入少量C02: C6H50+CO2+H20→C6H50H+HCO3- | |
| C. | 强碱性溶液中次氯酸钠溶液与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2Fe042-+3Cl-+H20+4H+ | |
| D. | 向 Ca(Cl0)2 溶液中通入过量 S02:Ca2++2C10-+SO2═CaSO4↓+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 浓硫酸的还原产物是SO2 | |
| B. | 该装置可随时控制反应的发生或停止 | |
| C. | ①中有白色固体生成,加水后溶液呈蓝色 | |
| D. | ②中盛放Ba(NO3)2溶液可吸收SO2,防止空气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
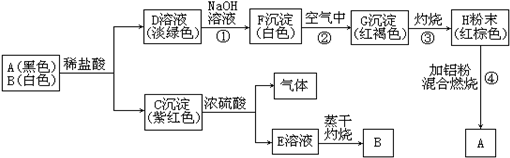
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20 g D2O所含的电子数为10 NA | |
| B. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1 NA | |
| C. | 1 mo1 Na被氧化成Na2O2,失去电子数目为2 NA | |
| D. | 氢气与氯气反应生成标准状况下22.4 L氯化氢,断裂化学键总数为2 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com