
| A. | 1:2 | B. | 3:1 | C. | 3:2 | D. | 4:3 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
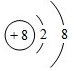 .
. ;含有离子键和共价键的化合物的化学式为Na2O2.
;含有离子键和共价键的化合物的化学式为Na2O2. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通常情况下氯气呈黄绿色,有刺激性气味,极易溶于水 | |
| B. | 氯气能够杀菌,常用于居室消毒 | |
| C. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| D. | 把集气瓶小心地放在鼻孔下直接闻氯气的气味 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com