【答案】
分析:A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,且C能形成单质C
2,所以C是N元素;B与D形成的化合物BD与C的单质C
2电子总数相等,且C的原子序数大于B小于D,所以B是C元素,D是O元素;CA
3分子结构为三角锥形,且A的原子序数小于B,所以A是H元素;D与E可形成E
2D与E
2D
2两种离子化合物,所以E是Na元素;D与F是同族元素,所以F是S元素.以此解答该题.
解答:解:A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,且C能形成单质C
2,所以C是N元素;B与D形成的化合物BD与C的单质C
2电子总数相等,且C的原子序数大于B小于D,所以B是C元素,D是O元素;CA
3分子结构为三角锥形,且A的原子序数小于B,所以A是H元素;D与E可形成E
2D与E
2D
2两种离子化合物,所以E是Na元素;D与F是同族元素,所以F是S元素.
(1)通过以上分析知,D是O元素,原子核外有8个电子,其核外电子排布图为:
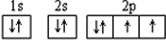
.
故答案为:
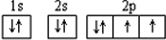
.
(2)化合物E
2F
2是离子化合物,和过氧化钠类似,钠离子和S
2-之间以离子键结合,硫原子和硫原子之间以共价键结合,所以其电子式
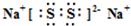
;化合物ABC是氢氰酸,结构式为
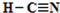
.
故答案为:

;
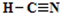
.
(3)杂化轨道数=σ键个数+孤电子对数.
BF
32-中心原子杂化轨道数=3+0=3,所以采取sp
2杂化;
D
3中心原子杂化轨道数=3,所以采取sp
2杂化;
FD
42-微粒中价层电子对数=4+0=4,所以它的VSEPR模型为正四面体,因为没有孤电子对,所以其空间构型为正四面体,键角是109°28′;FD
3分子中价层电子对数=3+0=3,所以它的VSEPR模型为平面三角形,因为没有孤电子对,所以其空间构型为平面三角形.
故答案为:sp
2杂化; sp
2杂化; 109°28′;平面三角形.
(4)与BD
2互为等电子体且含有C原子的微粒有N
2O、OCN
-或SCN
-或N
3-.
故答案为:OCN
-或SCN
-或N
3-.
(5)C
3H
7NO
2能与NaHCO
3溶液反应生成CO
2气体,说明该物质含有羧基,因为含有氮元素,所以还含有氨基,该分子具有手性,其结构简式为

;所有单键都是σ键,双键中含有一个σ键和一个π键,所以含有12个σ键1个π键.
故答案为:
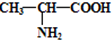
;12;1.
点评:本题考查了电子式的书写、分子的杂化方式、分子的空间构型等知识点,能正确推断元素是解本题的关键,分子的空间构型及杂化方式是高考的热点,应熟练掌握.

 .
. .
.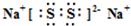 ;化合物ABC是氢氰酸,结构式为
;化合物ABC是氢氰酸,结构式为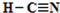 .
. ;
;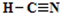 .
. ;所有单键都是σ键,双键中含有一个σ键和一个π键,所以含有12个σ键1个π键.
;所有单键都是σ键,双键中含有一个σ键和一个π键,所以含有12个σ键1个π键.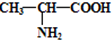 ;12;1.
;12;1.

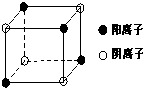 [化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.
[化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.