
【题目】某学习小组用下图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
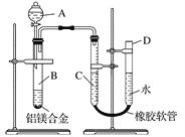
(1)A中试剂为________。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是___________。
(3)将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤、洗涤、干燥、称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B中滴加足量试剂;⑤检查气密性,上述操作的顺序是___________ (填序号);记录C的液面位置时,除视线平视外,还应__________。
(4)若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为________。
(5)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________(填“偏大”“偏小”或“不受影响”)。
【答案】NaOH溶液 除去铝镁合金表面的氧化膜 ⑤①④③② 使D和C中的液面相平 ![]() 偏小
偏小
【解析】
由于Mg、Al均可以和酸反应,因此不可以用酸来实验,由于Al可以和碱反应而Mg不反应,则可以用NaOH与Al反应制得H2,然后用排水法收集H2,以计算Al的量,据此解答。
(1)由于铝镁都能与酸反应放出氢气,但铝还能与碱(如NaOH溶液)反应放出氢气,而镁不能,要测定铝镁合金中铝的质量分数,应选择NaOH溶液,即A中试剂为NaOH溶液;
(2)铝镁的表面都容易形成一层氧化膜,在实验前必须除去,因此实验前,先将铝镁合金在稀酸中浸泡片刻的目的是除去铝镁合金表面的氧化膜;
(3)实验时,记下量气管中C的液面位置,再加入NaOH溶液开始反应,待反应完毕并冷却至室温后,记录量气管中C的液面位置,最后将B中剩余固体过滤,洗涤,干燥,称重,因此上述操作的顺序是⑤①④③②;量气管读数时为使里面气体压强与外界大气压相等,必须使D和C两管中液面相平;
(4)铝镁合金的质量为a g,B中剩余固体镁的质量为c g,则参加反应的铝的质量为(a-c)g,设铝的相对原子质量为M,则
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2M 3×22400mL
(a-c)g bmL
解得:M=33600(a-c)/b;
(5)铝的质量分数为:(a-c)/a,实验过程中,若未洗涤过滤所得的不溶物,c值偏大,铝的质量分数偏小。


科目:高中化学 来源: 题型:
【题目】某同学拟用氯化钙固体、碳酸钠溶液和稀硝酸等试剂,先制得碳酸钙,最终制得纯净的硝酸钙晶体。
(1)写出制取过程中反应的离子方程式:________________、________________________。
(2)请帮助该同学完成下列实验操作步骤(不要求回答使用的仪器)
①用蒸馏水完全溶解CaCl2后,加入________。
②将反应后的混合物过滤,并用适量蒸馏水洗涤沉淀至无Cl-。
③加入________________,使沉淀完全溶解。
④将所得溶液蒸发、结晶,得到纯净的硝酸钙晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用如图所示装置(甲、乙、丙三池中的溶质均足量)研究有关电化学的问题,当闭合该装置的开关K时,观察到电流表的指针发生了偏转。
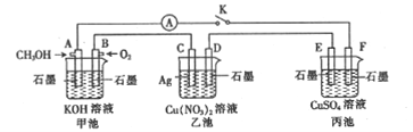
请回答下列问题:
(1)甲池为_______ (填“原电池”“电解池”或“电镀池”), A电极的电极反应式为_____.
(2)丙池中F电极为______(填“正极”“负极”“阴极”或“阳极”),该池中发生总反应的化学方程式为________
(3)若丙池中两端的电极不变,将其溶液换成NaCl溶液,则开关闭合一段时间后,丙池中溶液的PH将____(填“增大”“减小”或“不变”)。
(4)当乙池中C极质量减轻4.32 g时,甲池中B电极理论上消耗O2 的体积为____mL(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,采用了不同的实验方法(装置如图所示)。
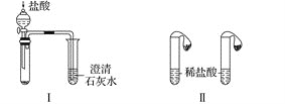
(1)根据上图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)____。
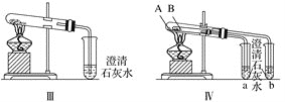
(2)图Ⅲ所示实验能够鉴别这两种物质,其反应的化学方程式为_______。
(3)图Ⅳ不仅能鉴别碳酸钠和碳酸氢钠,同时又能验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的物质为__________,实验过程中的现象为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图甲所示为二维平面晶体示意图,化学式表示为AX3的是________。

(2)图乙为一个金属铜的晶胞,请完成以下各题:
①该晶胞“实际”拥有的铜原子数是________个;
②该晶胞称为________(填序号);
A.六方晶胞 B.体心立方晶胞 C.面心立方晶胞
③此晶胞立方体的边长为a cm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则阿伏加德罗常数为________(用aρ表示)。
(3)《X射线金相学》中记载关于铜与金可形成两种有序的金属互化物,其结构如下图所示。下列有关说法正确的是________。
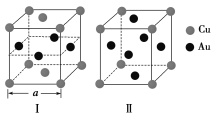
A.图Ⅰ、Ⅱ中物质的化学式相同
B.图Ⅱ中物质的化学式为CuAu3
C.图Ⅱ中与每个铜原子紧邻的铜原子有3个
D.设图Ⅰ中晶胞的边长为a cm,则图Ⅰ中合金的密度为![]() g·cm-3
g·cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,5-己二醇(C6H14O2)可以作为医药中间体和制备高分子聚合物的原料。2,5-已二醇和聚酯的合成路线如图所示:
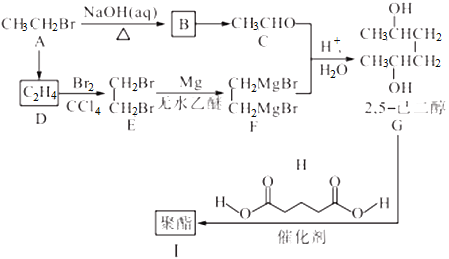
回答下列问题:
(1)A中所含官能团的名称为______,E的名称为______。
(2)D→E的反应类型是______,A→D的反应条件是______ 。
(3)A→B反应的化学方程式为______ 。
(4)G→I反应的化学方程式为______ 。
(5)物质H的同分异构体有多种,同时满足下列三个条件的共有___种,其中核磁共振氢谱为三组峰的是______ (写结构简式)。
①能发生银镜反应;②能与碳酸氢钠溶液反应;③能发生水解反应。
(6)参照上述合成路线,以苯和乙醛为原料(其他试剂任选),设计制备苯乙烯的合成路线。______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有10 g Na2O2、Na2O、Na2CO3、NaOH的混合物与200 g质量分数为3.65%的盐酸恰好反应,蒸干溶液,最终得固体NaCl质量为
A. 11.7 g B. 5.85 g
C. 8 g D. 15.5 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用某废催化剂(主要成分Al2O3、K2O、少量CoO、SiO2等)来制取明矾的工艺流程如下图所示,回答下列问题:

(1)废催化剂在浸取前进行球磨的主要目的是________________________________________。
(2)浸取时Al2O3溶解的化学方程式为________________________________________;
(3)滤渣的主要成分是_________________ (填化学式)。
(4)实验测得K2CO3的加入量与KA1(SO4)2·12H2O产率及纯度关系如下表所示:
编号 | 1 | 2 | 3 | 4 |
K2CO3加入量/g | 2 | 4 | 6 | 8 |
产品质量/g | 3.3 | 5.7 | 4.6 | 4.5 |
明矾纯度/g | 99.1 | 98.2 | 91.4 | 84.9 |
当K2CO3的加入量超过4 g后,晶体的质量减少且纯度降低,其原因是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com