
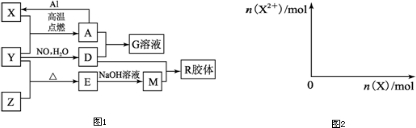
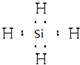 ,
,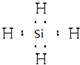 ;
;| xmol×2 |
| 3 |
| xmol×2 |
| 3 |
 ,
, .
.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
| A、FeCl2中有CuCl2 (铁粉) |
| B、KCl中有杂质K2SO4(氯化钡) |
| C、N2中混有O2(灼热的铜粉) |
| D、CO2中混有HCl(氢氧化钠溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、20℃时,饱和KCl溶液与等质量的水混合后物质的量浓度大于2.0mol?L-1 |
| B、20℃时,将29.8 gKCl溶于87.6g水中可得饱和溶液 |
| C、20℃时,密度小于1.174g?cm-3的KCl溶液是不饱和溶液 |
| D、将此溶液蒸发部分水,再恢复到20℃时,溶液中各离子的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.2升 |
| B、67.2升 |
| C、4.48升 |
| D、33.6升 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液.如图是医院病人输液使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签
为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液.如图是医院病人输液使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com