
| A.酸式滴定管未润洗 | B.酸式滴定管滴定前有气泡,滴定后气泡消失 |
| C.配制盐酸标准液时,定容俯视 | D.乙酸乙酯未完全水解 |
 CH3COO CH2CH3 +H2O(浓硫酸加热) (2分)
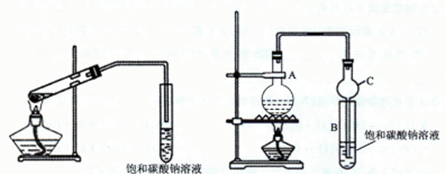
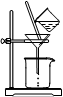
CH3COO CH2CH3 +H2O(浓硫酸加热) (2分) CH3COO CH2CH3 +H2O,饱和碳酸钠溶液的作用有:?乙酸乙酯在无机盐碳酸钠饱和溶液中溶解度小;?碳酸钠能跟挥发出的乙酸反应。而NaOH碱性较强,将促使乙酸乙酯水解。图1中导管容易发生倒吸,而图2导管具有防倒吸功能。NaOH与乙酸乙酯发生反应:CH3COOCH2CH3+NaOH=CH3COONa+CH3CH2OH,使用盐酸测量NaOH的剩余量,可知NaOH的消耗量,省略本题简单计算。滴定NaOH使用的指示剂是酚酞溶液,酚酞遇碱变红,遇酸无色。
CH3COO CH2CH3 +H2O,饱和碳酸钠溶液的作用有:?乙酸乙酯在无机盐碳酸钠饱和溶液中溶解度小;?碳酸钠能跟挥发出的乙酸反应。而NaOH碱性较强,将促使乙酸乙酯水解。图1中导管容易发生倒吸,而图2导管具有防倒吸功能。NaOH与乙酸乙酯发生反应:CH3COOCH2CH3+NaOH=CH3COONa+CH3CH2OH,使用盐酸测量NaOH的剩余量,可知NaOH的消耗量,省略本题简单计算。滴定NaOH使用的指示剂是酚酞溶液,酚酞遇碱变红,遇酸无色。

科目:高中化学 来源:不详 题型:单选题
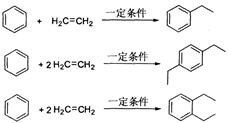
| A.乙烷与氯气混合 | B.乙烯与氯化氢气体混合 |
| C.乙烯与氯气混合 | D.乙烯通入浓盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 装置 | A | B | C | D |
| 试剂 | FeCl2溶液 | 淀粉KI溶液 | 石蕊溶液 | |
| 现象 | 溶液由浅绿色变为棕黄色 | | | |
| 离子方程式 | | | | |
| 装置 | A | B | C |
| 试剂 | 品红溶液 | 酸性高锰酸钾溶液 | 硫化氢的水溶液 |
| 现象 | | 紫色退去 | |
| 体现SO2的性质 | | | 氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将5.85gNaCl固体溶于1 L水中可配成0.1 mol·L-1的NaCl溶液 |
| B.定容时仰视观察液面,实验结果偏低 |
| C.固体溶解后,将溶液转移到容量瓶中,然后向容量瓶中直接加水稀释到刻度线 |
| D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将pH试纸用蒸馏水湿润后测某溶液的pH |
| B.配制500mL 0.10mol/L NaCl溶液,定容时俯视 |
| C.以标准盐酸溶液滴定未知浓度的NaOH溶液时,酸式滴定管未用标准溶液润洗 |
| D.用标准NaOH溶液滴定未知浓度的盐酸溶液,开始时滴定管尖嘴处没有气泡,结束时有气泡 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com