
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答有关问题。
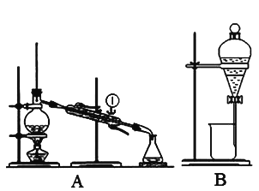

(1)装置A中①的仪器名称是____________。利用装置B分液时为使液体顺利滴下,应进行的具体操作是____________。
(2)从氯化钾溶液中得到氯化钾固体,应选择装置__________(填字母,下同);除去自来水中的![]() 等杂质,应选择装置________。
等杂质,应选择装置________。
(3)从碘水中分离出![]() ,应选择装置_____________,该分离方法的名称为____________。
,应选择装置_____________,该分离方法的名称为____________。
【答案】(直形)冷凝管 将上端玻璃塞打开,再旋转下面的旋塞 C A B 萃取
【解析】
(1)根据图示判断仪器名称;利用装置B分液时为使液体顺利滴下,需要使分液漏斗内液面上的气体与空气相通,据此分析解答;
(2)从氯化钾溶液中得到氯化钾固体,为可溶性固体与液体分离;除去自来水中的Cl-等杂质,可以利用水容易挥发的性质分离;
(3)碘不易溶于水,易溶于有机溶剂,据此分析解答。
(1)由图可知仪器①的名称是冷凝管;利用装置B分液时为使液体顺利滴下,应先将分液漏斗上部的玻璃塞打开或使塞子上的凹槽与口部瓶壁的小孔对齐,再旋开分液漏斗的旋塞,故答案为:冷凝管;将分液漏斗上部的玻璃塞打开,再旋开分液漏斗的旋塞;
(2)从氯化钾溶液中得到氯化钾固体,为可溶性固体与液体分离,选择蒸发装置,即C装置;除去自来水中的Cl-等杂质,可以通过蒸馏实现,选用蒸馏装置,即A装置,故答案为:C;A;
(3)碘不易溶于水,易溶于有机溶剂,则从碘水中分离出I2,可以利用萃取法分离,应选择装置B,故答案为:B;萃取。


科目:高中化学 来源: 题型:
【题目】最近有科学家研发了一种新型锂空气电池,结构如下图所示。已知:①电解质由离子液体(离子能够自由移动,非溶液)和二甲基亚砜[(CH3)2SO]混合制成,可促进过氧化锂生成;②碳酸锂薄层的作用是让锂离子进入电解质,并阻止其它化合物进入该电极;③二硫化钼起催化作用。该装置工作时,下列叙述不正确的是

A. 放电时,a极发生氧化反应
B. 放电时的总反应为:2Li+O2=Li2O2
C. 充电时,Li+在电解质中由b极移向a极
D. 充电时,b极的反应式:Li2O2+2e-=2Li+O22-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
A. 溶液中导电粒子的数目增加,导电性增强
B. 醋酸的电离程度增大,pH增大
C. 再加入10mLpH=11NaOH溶液,混合液pH>7
D. 溶液中c(CH3COO—)/c(CH3COOH)c(OH—)变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH3COONa溶液存在水解平衡:CH3COO-+H2O![]() CH3COOH+OH-,下列说法正确的是( )
CH3COOH+OH-,下列说法正确的是( )
A. 稀释溶液,溶液的pH增大 B. 加入少量NaOH固体,c(CH3COO-)减小
C. 温度升高,c(CH3COO-)增大 D. 加入少量FeCl3固体,c(CH3COO-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Co3O4是一种电极材料,可用草酸盐湿式沉淀—煅烧分解法制备。
(1)先用(NH4)2C2O4溶液和CoCl2溶液为原料制取难溶于水的CoC2O4·2H2O晶体。
①已知25 ℃,Kb(NH3·H2O)=1.8×10-5,H2C2O4的Ka1=5.6×10-2,Ka2=5.4×10-5。(NH4)2C2O4溶液的pH__ (填“>”“=”或“<”)7。
②反应时,使(NH4)2C2O4过量的原因是________________________。
(2) 为确定由CoC2O4·2H2O获得Co3O4的最佳煅烧温度,准确称取4.575 g的CoC2O4·2H2O样品,在空气中加热,固体样品的剩余质量随温度的变化如图所示(已知385 ℃以上残留固体均为金属氧化物)

①B处的物质为________(填化学式)。
②经测定,205~385 ℃的煅烧过程中,产生的气体为CO2,计算AB段消耗O2在标准状况下的体积。(写出计算过程,结果保留2位有效数字) ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101kPa条件下,将15L O2通往10L CO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15L,则原CO和H2的混合气体中,V(CO)=__________L,V(H2)=___________L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气中,V(CO): V(H2)=_______。
(3)若剩余气体的体积为a L,则a的取值范围是_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)在下列化学方程式中,双线桥法标出电子转移并填空。3S+6KOH![]() K2SO3+2K2S+3H2O___,氧化剂___,还原剂___;2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑___,氧化剂___,被氧化的物质_____;3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O___,被还原的物质_____,还原剂______。
K2SO3+2K2S+3H2O___,氧化剂___,还原剂___;2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑___,氧化剂___,被氧化的物质_____;3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O___,被还原的物质_____,还原剂______。
(2)请把符合要求的化学反应方程式的编号填入括号内:是分解反应又是氧化还原反应的是___,是分解反应不是氧化还原反应的是___,是化合反应又是氧化还原反应的是___,是化合反应不是氧化还原反应的是___,不属于四种基本反应类型的氧化还原反应的是___。
A.2KClO3![]() 2KCl+3O2↑ B.2Fe+3Cl2
2KCl+3O2↑ B.2Fe+3Cl2![]() 2FeCl3 C.NH4HCO3
2FeCl3 C.NH4HCO3![]() NH3↑+H2O+CO2↑D.CaO+CO2=CaCO3 E.Cl2+H2O=HCl+HClO
NH3↑+H2O+CO2↑D.CaO+CO2=CaCO3 E.Cl2+H2O=HCl+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1为“镁﹣次氯酸盐”燃料电池原理示意图。图2为“双极室成对电解法”生产乙醛酸原理示意图,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。下列说法不正确的是

A. 若利用镁燃料电池为电源,则E极连M极
B. 镁燃料电池负极容易与水发生自腐蚀产生氢气
C. F电极上的电极反应式为ClO-+2e-+H2O=Cl-+2OH-
D. 图2装置中若有2 mol H+通过质子交换膜完全反应,则共生成2 mol乙醛酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com