
【题目】在容积为2L的密闭容器中充入3mol气体A和2.5mol气体B,发生反应:3A(g)+B(g)![]() xC(g)+2D(g).5min以后,测得生成1mol D,C的平均反应速率v(C)=0.1mol/(L·min).试求:
xC(g)+2D(g).5min以后,测得生成1mol D,C的平均反应速率v(C)=0.1mol/(L·min).试求:
(1)方程式中C的化学计量数x=________。
(2)5min内A的平均反应速率v(A)=________。
(3)5min时B的转化率为________。
(4)温度升高A的转化率________(填“增大”、“减小”或“不变”);压强增大B的转化率________。
【答案】 2 0.15 mol·L-1·min-1 20% 增大 不变
【解析】C的平均反应速率v(C)=0.1molL﹣1min﹣1,反应生成C物质的量=0.1molL﹣1min﹣1×2L×5min=1mol;
3A(g)+B(g)xC(g)+2D(g)
起始量(mol) 3 2.5 0 0
变化量(mol) 1.5 0.5 0.5x 1
平衡量(mol) 1.5 2 0.5x 1
(1)上述计算结合反应生成的C物质的量计算得到x,0.5x=1,x=2;
(2)5min内A的平均反应速率=![]() =
= =0.15mol/Lmin;
=0.15mol/Lmin;
(3)5min时B的转化率=![]() ×100%=
×100%=![]() ×100%=20%;
×100%=20%;
(4)由题意可知,正反应为吸热反应,所以升高温度,平衡向正反应方向移动,所以A的转化率增大,由(1)计算得x=2,所以该反应为气体体积不变的反应,增大压强,平衡不移动,所以B的转化率不变,


科目:高中化学 来源: 题型:
【题目】下列关于乙酸的说法中,错误的是
A. 乙酸是一种重要的有机酸,常温下是具有刺激性气味的液体
B. 乙酸的分子式为C2H4O2,与甲酸(HCOOH)互为同系物
C. 乙酸不能被酸性高锰酸钾稀溶液氧化
D. 乙酸官能团的结构式为-COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由两种短周期元素组成的化合物XY3,若两种元素的原子序数分别为a和b,则a和b的关系正确的是
①a=b+4;②a+b=8;③a+b=30;④a=b+8
A. 1个 B. 2个 C. 3个 D. 4个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将amol/L Al2(SO4)3和钾离子浓度为2bmol/L的K2SO4混合溶液500mL加水稀释到2L,则稀释后的溶液中SO42﹣的浓度为( )
A.![]() ?mol/L
?mol/L
B.4(3a+b) mol/L
C.4(a+b) mol/L
D.![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)某气体的分子为双原子分子,其摩尔质量为M gmol﹣1 , 现有标准状况下V L该气体,设阿伏加德罗常数的值为NA , 则:
①该气体的物质的量为 mol;
②该气体中所含的原子总数为;
③该气体在标准状况下的密度为 gL﹣1;
④该气体的一个分子的质量为 g.
(2)气体化合物A分子式可表示为OxFy , 已知同温同压下10mL A受热分解生成15mL O2和10mL F2 , 则A的化学式为 , 推断的依据为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20.0g质量分数为14.0%的KNO3溶液与30.0g质量分数为24.0%的KNO3溶液混合,得到的密度为1.15g/cm3的混合溶液.计算:
(1)混合后溶液的质量分数.
(2)混合后溶液的物质的量浓度.
(3)在1 000g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用一种微生物可将废水中苯酚的化学能直接转化为电能,装置如图所示。电池工作时,下列说法正确的是
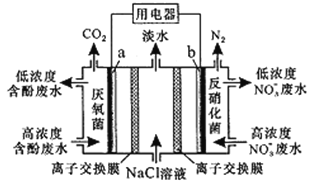
A. a为正极,发生氧化反应
B. b极上的电极反应为:2NO3-+12H+-10e-=N2↑+6H2O
C. 中间室的Cl-向左室移动
D. 左室消耗苯酚(C6H5OH)9.4g时,用电器流过2.4mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)9.8克SO42﹣的物质的量为 , 质子数为个(用NA表示)
(2)在3S+6KOH═2K2S+K2SO3+3H2O的反应中,氧化剂还原剂 , 氧化剂与还原剂的质量之比为 .
(3)在标准状况下,33.6L的NH3将其溶解于水配成1L的溶液,则溶液的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同温同压下,下列各组热化学方程式中,Q2>Q1的是(双选)( )
A. 2H2(g)+O2(g)===2H2O(g) ΔH=-Q1
2H2(g)+O2(g)===2H2O(l) ΔH=-Q2
B. S(g)+O2(g)===SO2(g) ΔH=-Q1
S(s)+O2(g)===SO2(g) ΔH=-Q2
C. C(s)+1/2O2(g)===CO(g) ΔH=-Q1
C(s)+O2(g)===CO2(g) ΔH=-Q2
D. H2(g)+Cl2(g)===2HCl(g) ΔH=-Q1
1/2H2(g)+1/2Cl2(g)===HCl(g) ΔH=-Q2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com